
Revisión | Respirar, 2026; 18 (1): 172-184 | ISSN 2953-3414 | https://doi.org/10.55720/respirar.18.1.13
¿La EPOC y sus exacerbaciones tienen un real impacto sobre la salud cardio y cerebrovascular? ¿Este impacto es modificable?
Does COPD and its Exacerbations Truly Impact Cardiovascular and Cerebrovascular Health? Is this Impact Modifiable?
1 Centro de Investigaciones en Patologías Respiratorias, San Miguel de Tucumán, Tucumán, Argentina.
2 Universidad Buenos Aires, Facultad de Medicina, Hospital “Dr. J. M. Ramos Mejia”, Unidad de Neumotisiología, Ciudad de Buenos Aires, Argentina
3 Centro Médico Capital, Servicio de Medicina Respiratoria, La Plata, Provincia de Buenos Aires, Argentina.
4 Sanatorio San Roque, Servicio de Neumonología, Curuzú Cuatiá, Corrientes, Argentina.
5 Universidad de Buenos Aires, Facultad de Medicina, Carrera de Médico Especialista de Neumonología, Buenos Aires, Argentina.
Autor corresponsal:
Martín Sívori E-mail: sivorimartin@yahoo.com
Unidad de Neumotisiología, Urquiza 609, Código Postal 1405, Ciudad Autónoma de Buenos Aires.
Recibido:
13 septiembre 2025
Aprobado:
30 octubre 2025
Resumen
En Argentina, el tabaquismo causa más de 47.000 muertes anuales por cáncer, enfermedades cardiovasculares (ECV), enfermedad pulmonar obstructiva crónica (EPOC), neumonía y accidente cerebrovascular (ACV). Aproximadamente 7.000 personas mueren anualmente por EPOC en Argentina. Afecta al 14,5% de >40 años, con subdiagnóstico preocupante. Se realizó una revisión narrativa de las principales bases de datos científicos entre 1996 y 2025. El objetivo de este artículo es analizar las razones por las cuales la EPOC y sus exacerbaciones son factores de riesgo para ECV y ACV, y las estrategias preventivas que han disminuido riesgos.
Los pacientes con EPOC tienen mayor prevalencia de ECV y su severidad se correlaciona con mayor riesgo de muerte cardiovascular y general. Las infecciones respiratorias agudas, como influenza, virus sincicial respiratorio (VSR), SARS-CoV-2 y el Streptococcus pneumoniae, asociadas a las exacerbaciones de EPOC “per se”, aumentan significativamente el riesgo de eventos cardiovasculares y cerebrovasculares. Las exacerbaciones de EPOC incrementan drásticamente la morbimortalidad cardiovascular y cerebrovascular hasta un año después del evento.
Para prevenir el impacto cardio-cerebrovascular en pacientes con EPOC, son cruciales varias intervenciones. La cesación tabáquica es la más costo-efectiva, reduciendo la mortalidad. La rehabilitación respiratoria y la actividad física regular mejoran la salud y disminuyen la mortalidad general, cardiovascular y respiratoria. La vacunación contra influenza y neumococo reducen el riesgo de eventos cardiovasculares mayores y mortalidad. Finalmente, la triple terapia inhalada en pacientes EPOC exacerbadores con > 300 eosinófilos/ul reduce la mortalidad y eventos cardiovasculares.
Palabras claves: EPOC; enfermedad cardiovascular; enfermedad cerebrovascular; exacerbación; prevención.
Abstract
In Argentina, tobacco consumption causes over 47,000 deaths annually, primarily due to cancer, cardiovascular diseases (CVD), chronic obstructive pulmonary disease (COPD), pneumonia, and stroke (CVA). Nearly 7,000 people die from COPD in Argentina each year. It affects 14.5% of Argentinians over 40, with a concerning rate of underdiagnosis. A narrative review of the main scientific databases was conducted between 1996 and 2025. This article aims to analyze why COPD and its exacerbations are risk factors for CVD and CVA, and the preventive strategies that have shown to reduce these risks.
Patients with COPD have a higher prevalence of CVD, and its severity correlates with an increased risk of cardiovascular and overall mortality. Acute respiratory infections, such as influenza, respiratory syncytial virus (RSV), SARS-CoV-2, and Streptococcus pneumoniae, associated with COPD exacerbations “per se”, significantly increase the risk of cardiovascular and cerebrovascular events. COPD exacerbations drastically raise cardiovascular and cerebrovascular morbidity and mortality for up to a year after the event.
To prevent cardiovascular and cerebrovascular impact in patients with COPD, several interventions are crucial. Smoking cessation is the most cost-effective intervention, reducing mortality. Respiratory rehabilitation and regular physical activity (over 10,000 steps daily) improve health and decrease overall, cardiovascular, and respiratory mortality. Vaccination against influenza and pneumococcus significantly reduces the risk of major cardiovascular events and mortality. Finally, inhaled triple therapy in frequent COPD exacerbator patients with >300 eosinophils/µl has shown to reduce mortality and cardiovascular events.
Key words: COPD; cardiovascular disease; cerebrovascular disease; exacerbation; prevention.
Introducción
En Argentina, el tabaquismo produce más de 47.000 muertes anuales por cáncer, enfermedad cardiovascular (ECV), enfermedad pulmonar obstructiva crónica (EPOC), neumonía, accidente cerebrovascular (ACV), entre otras.1 La EPOC es la tercera causa mundial de mortalidad (Organización Mundial de la Salud-OMS-).2 Aproximadamente, 7.000 personas mueren anualmente por EPOC en Argentina y su prevalencia es en >40 años de 14,5%, con alto subdiagnóstico (77,4%).3,4
El objetivo de esta revisión es analizar las razones por las cuales la EPOC y sus exacerbaciones son factores de riesgo para enfermedades cardio y cerebrovasculares (ECEV) y las estrategias preventivas que disminuyen sus riesgos.
Materiales y métodos
Se realizó una revisión narrativa en diferentes bases de datos como Pubmed, Embase, Web of Sciences, Cochrane Library, Scopus, SciELO, Lilacs, entre 1996 y 2025, y se eligieron aquellas referencias que a juicio de los autores sus conclusiones aportaban al objetivo propuesto.
1. El tabaquismo como causa común de enfermedades
Dentro de los etiotipos de la EPOC, el tabaquismo es la principal causa en el mundo de ECEV.1,5 Se lo relaciona a mayor riesgo de infecciones respiratorias.6-7 En un meta-análisis (nueve estudios, n=40.685), se demostró que los fumadores actuales tienen cinco veces más riesgo de influenza.6 En otro metanálisis (veinte estudios, n=1.812), se determinó que los fumadores actuales tienen una razón de momios, o razón de ventajas, o razón de productos cruzados (Odds Ratio, OR) mayor de hospitalizaciones de 1,5, (IC95% 1,3-1,7) y hospitalizaciones en Unidad de Cuidados Intensivos (UTI) de OR 2,2, (IC95% 1,4-3,4).7 En la Tabla 1 se presentan los pacientes con EPOC y su vínculo con su condición de tabaquistas actuales o ex-tabaquistas.4
Tabla 1.
Relación de condición de tabaquismo en pacientes con EPOC en el estudio EPOC.AR.4
|
Variables |
Total (n=504) |
% |
|---|---|---|
|
Fumador actual |
219 |
43 |
|
Ex-fumador |
193 |
38,3 |
|
Nunca fumó |
92 |
18,3 |
2. Conceptos de sindemia y comorbilidad
El concepto de sindemia se usó por primera vez en 1996.8 Durante la pandemia de COVID-19, se retomó para significar que era una “sinergia de epidemias”.9 Señala entonces a dos o más enfermedades muy prevalentes, epidémicas, que se relacionan fisiopatológicamente entre sí, retroalimentándose sus riesgos de morbilidad y mortalidad, agravadas por factores sociales, económicos y ambientales. Solidoro et al. introdujeron el término de enfermedades “sindémicas” para EPOC y su asociación con otras enfermedades relacionadas.10
En cambio, el concepto de comorbilidad se refiere a que cada enfermedad se considera independientemente, aunque puedan concurrir temporalmente, pero no necesariamente fisiopatológicamente.
Las ECV son la principal causa de morbimortalidad en todo el mundo.11 Se ha determinado que la prevalencia en EPOC de ECV fue mayor vs. control (n=17.384) (56,5% vs 25,6%, p< 0,0001), OR 2,7, (IC 95% 2,3–3,2).12 La EPOC tuvo mayor riesgo de enfermedad coronaria (OR 2, IC95%, 1,5–2,5), angina (OR 2,1, IC95%, 1,6–2,7), infarto agudo de miocardio (IAM) (OR 2,2, IC95%, 1,7–2,8), ACV (OR 1,5, IC95%, 1,1–2,1), insuficiencia cardíaca (ICC) (OR, 3,9, IC95% 2,8–5,5) y arritmias (OR 2,4, IC95%, 2,0–2,8).12
En nuestro país, en una cohorte de pacientes con EPOC (n=354), las comorbilidades más frecuentes fueron hipertensión (HTA) 24,2%, ICC 12,4%, diabetes (DBT) 8,2%, cáncer 7,3% y síndrome de superposición asma-EPOC 3,6%, siendo más frecuente en pacientes con obstrucción moderada a grave y GOLD B/E.13
Recientemente, se describió la alta prevalencia de enfermedad coronaria por angiotomografía (88%), la mayoría desconocida (OR 3,1, IC95%, 1,1–8,9, p= 0,037), y más extensa en aquellos con biomarcadores inflamatorios sistémicos (fibrinógeno, proteína-C-reactiva), engrosamiento de la pared bronquial y crecimiento bacteriano en el esputo.14
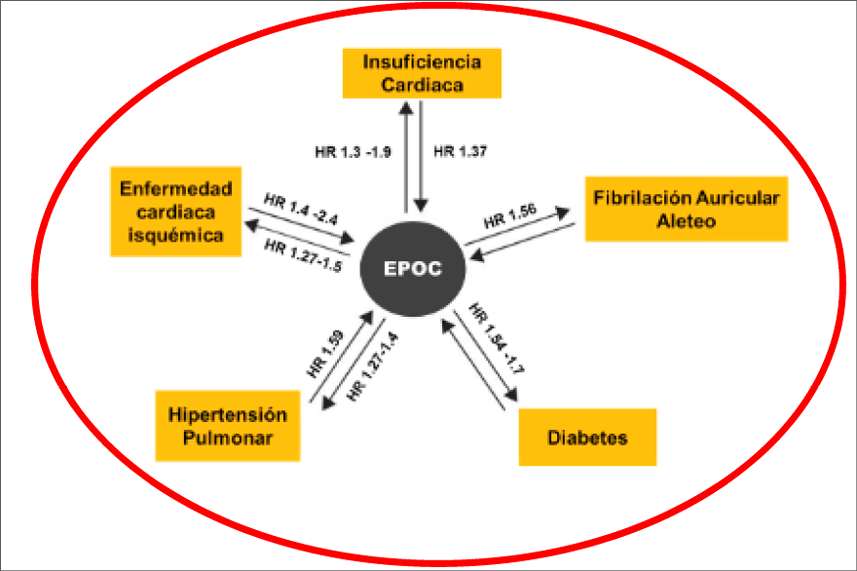
En la Figura 1, se resumen las relaciones entre la EPOC y enfermedades sindémicas.15
La EPOC y su severidad por obstrucción bronquial es factor de riesgo de ACV, aunque se discute el mecanismo que las relaciona.12,16 Se han postulado al tabaquismo, infecciones, hipoxemia, hipercapnia, enfermedades asociadas (HTA, FA, ICC, coronaria), edad y disminución de la actividad física.17
Figura 1.
Enfermedades sindémicas15
3. EPOC y causas de muerte
La ECV ha sido causa de mortalidad en estudios clínicos que van del 16% (UPLIFT) al 39% (EUROSCOP).18 Mannino et al. (n=15.759), ajustando por covariables todas las categorías GOLD, observaron mayor predicción de mortalidad, a mayor estadio GOLD.19 La muerte cardiovascular fue más incidente en GOLD II y la respiratoria en III-IV.19 Soler Cataluña et al. a 5 años determinaron que 38,2% de los pacientes fallecieron por causas respiratorias (25,7%), cardiovasculares (3,9%), cerebrovasculares (2,3%) y neoplasias (3,6%).20
En conclusión, la contigüidad y continuidad anátomo-fisiológica del sistema respiratorio y cardiovascular fundamentan que la alteración en sus funciones de cualquiera de ellos se pueden afectar mutuamente.21
4.Riesgos cardiovasculares y cerebrovasculares luego de una exacerbación de EPOC (Tabla 3A)
La definición actual de exacerbación requiere de la evaluación de criterios clínicos, cambios en el examen físico, oximetría y laboratorio.5 A pesar de la subestimación por parte de los médicos y de los pacientes, la exacerbación de la EPOC es un evento desfavorables de la EPOC, similar al IAM en pacientes con enfermedad coronaria. (Tabla 2) Los factores de riesgo más prevalentes de exacerbación de EPOC son: tabaquismo, grado de obstrucción bronquial y antecedente de una exacerbación.5 La mortalidad intrahospitalaria de una exacerbación de EPOC es 5-10%.5 Luego de una hospitalización por exacerbación de EPOC, la mortalidad es 11,3% posterior a 90 días del alta.22 Existe una tasa alta de rehospitalizaciones (25-30%).5 Soler Cataluña et al. han demostrado que la mortalidad a 5 años depende del número y severidad de las exacerbaciones.8 El estudio EXACOS determinó la epidemiología de las exacerbaciones graves y su manejo en países de ingresos bajos y medianos.23 La prevalencia anual de exacerbaciones graves fue 20,1%, y 48,4% experimentaron más de una exacerbación grave en los cinco años previos, disminuyendo el intervalo inter-exacerbaciones a medida que aumentaba su frecuencia.23
Tabla 2.
Similitudes entre el infarto agudo de miocardio y la exacerbación de EPOC.
|
Enfermedad coronaria (IAM) |
EPOC (Exacerbación) |
|
|---|---|---|
|
Mayores síntomas |
✔ |
✔ |
|
Mayores hospitalizaciones |
✔ |
✔ |
|
Peor calidad de vida |
✔ |
✔ |
|
Peor tolerancia al ejercicio |
✔ |
✔ |
|
Peor pronóstico |
✔ |
✔ |
IAM: Infarto agudo de miocardio
EPOC: Enfermedad pulmonar obstructiva crónica
Las exacerbaciones pueden generar un gran deterioro de la calidad de vida y mayor fragilidad. Esta se refiere a un estado de vulnerabilidad creciente asociado al envejecimiento, caracterizado por disminución de las reservas fisiológicas y funcionales, lo que incrementa el riesgo de caídas, discapacidad, dependencia, institucionalización y muerte.22
Los mecanismos fisiopatológicos que vincularían el mayor riesgo cardiovascular y la exacerbación de EPOC estarían dados por: hipoxemia, inflamación sistémica que favorece la disfunción ventricular y daño aterosclerótico vascular y sistémico, hiperinsuflación que reduce el gasto cardíaco, alteración ventilación/perfusión, insuficiente entrega de oxígeno tisular, estrés oxidativo, estado de hipercoagulabilidad, hipertensión pulmonar y activación simpática.24
Diversos estudios retrospectivos han generado nuevas hipótesis sobre un mayor riesgo futuro de ECEV tras una exacerbación moderada ocurrida en el año previo, las cuales deberán ser confirmadas mediante estudios prospectivos, como cohortes.25-27 Donaldson et al. determinaron que luego de una exacerbación moderada el riesgo de IAM se duplicó en los primeros 5 días y aumentó 40% el riesgo de ACV en los primeros 10 días.25 Incluso en los grupos GOLD A y B, no impresionaría que es lo mismo tener o no una exacerbación moderada en el año previo.28
Dos estudios prospectivos, un análisis sistemático, dos metanálisis y un Consenso Delphi brindan información adicional valiosa.29-33 En el estudio SUMMIT, los riesgos de ECV persistieron hasta un año luego de una exacerbación moderada y grave: 1-30 días: razón de riesgos o Hazard Ratio (HR) 3,8 (IC95%, 2,7-5,5), 31-90 días riesgo HR 1,9 (IC95% 1,3-2,7), 91-365 días HR 1,9 (IC95% 1,5-2,4) y más allá de 365 días HR 1,2 (IC95% 0,8-1,7). Si sólo se tomaban las exacerbaciones graves, el riesgo al primer mes aumentó 10 veces.29 En el estudio EXACOS-CV se observó que el riesgo de mortalidad cardiovascular o global fue más de 20 veces mayor en los primeros 7 días de hospitalización y permaneció elevado hasta el año.30 En un meta-análisis (82 estudios, n=18 millones de pacientes con enfermedad coronaria), la prevalencia de EPOC fue 12% (IC95%: 9,9%–14,1%).31 Se observó incremento de la posibilidad de ECV (OR 0,50, IC95% 0,38–0,66), mayor mortalidad hospitalaria (OR 1,47, IC95% 1,37–1,58), eventos mayores cardiovasculares (OR 1,81, IC95% 1,44–2,27), ICC (OR 2,14, IC95% 1,86–2,46), shock cardiogénico (OR 1,3, IC95% 1,01–1,68) y mortalidad a largo plazo (OR 1,99, IC95% 1,8–2,2).31 Un Consenso Delphi del Reino Unido de once neumólogos y cardiólogos definió a las exacerbaciones de EPOC como un importante problema de salud pública, con alta mortalidad y consumo de recursos de salud y costos, asociados a ECEV.32Pirera et al. en otro metanálisis de 16 estudios (1,8 millones de pacientes) determinaron la mayor incidencia de enfermedad coronaria aguda, ICC, ACV y arritmias, especialmente en los primeros 30 días luego de una exacerbación.33 El riesgo disminuyó progresivamente hasta el año a excepción de la enfermedad coronaria aguda que permaneció persistentemente elevada más allá del año, y el riesgo de ICC fue mayor que el resto de los eventos.33Se ha propuesto reclasificar a GOLD B y E según estén presentes las ECV (B+ y E+).34
En conclusión, existen crecientes evidencias del incremento de la morbimortalidad de ECV posterior a una exacerbación grave de EPOC. A partir de estudios retrospectivos, impresionaría que el haber padecido una sola exacerbación moderada también expone a mayor riesgo de mortalidad futura (menor certeza de evidencia).5 La matriz B está compuesta por individuos con mucha comorbilidades y mortalidad importante.5,35
Tabla 3. A.
Relaciones entre EPOC, exacerbaciones e impacto en los eventos cardio- cerebrovasculares y mortalidad.
|
Autores |
Año |
Diseño |
Resultados |
|---|---|---|---|
|
Global Burden Disease 2015 Study11 |
2016 |
Estudio de base de datos de 249 causas de muertes en 195 países entre 1980-2015. EPOC vs. control |
Prevalencia ECV EPOC 56,1% vs 25,6% (OR 2,7, IC 95% 2,3-3,2) (p<0,001) |
|
Finkelstein et al. 12 |
2009 |
Estudio de base de datos de 2002 de Estados Unidos de sujetos>40 años (n= 18.342) del National Health Interview Survey (NHIS). EPOC vs. control |
Riesgo enfermedad coronaria OR 2 (IC 5% 1,5-2,5); angina OR 2,1 (IC 95% 1,6-2,7); IAM OR 2,2 (IC 95% 1,7-2,8); ACV OR 1,5 (IC 95% 1,1-3,1); ICC OR 3,9 (IC 95% 2,8-5,5); arritmias OR 2,4 (IC 5% 2-2,8) |
|
Mac Leod et al.14 |
2025 |
Estudio caso EPOC-control prospectivo, asintomáticos por angiotomografía para detectar enf. coronaria |
Prevalencia enfermedad coronaria: 8,8% (OR 3,1; IC 95% 1,1-8,9) (p=0,037) |
|
Kunisaki et al.29 |
2018 |
Estudio SUMMIT prospectivo, controlado, (n=16.485 con factores de riesgo cardiovascular) evaluó el impacto sobre la mortalidad y eventos cardiovasculares mayores de furoato de fluticasona y vilanterol combinados vs. monoterapias |
Riesgo luego exacerbación moderada de ECV: 1 a 30 días HR 3,8 (2,7-5,5); 31-0 días: HR 1,9 (1,3- 2,7); 91-365 días HR 1,9 (1,5-2,4); >365 días HR 1,2 (0,8-1,7) |
|
Daniels et al.30 |
2024 |
Estudio EXACOS-CV Cohorte retrospectiva en Estados Unidos entre 2012-19 Sobre 435.925 pacientes con EPOC que 170.236 tuvieron ≥1 exacerbación. |
Riesgo de mortalidad se incrementó durante 2 años después de una exacerbación en especial en los primeros 30 días HR 1,79 (IC 95% 1,58-2,04); para exacerbación moderada HR 1,22 (IC 95% 1,04-1,.43); grave HR 5,09 (IC 95% 4,30-6,03). Riesgos de ECV se incrementaron durante 1 año post-exacerbación y máximos en los primeros 30 días para cualquier exacerbación HR 1,34 (IC 95% 1,23-1,46); moderada HR 1,23 (IC 95% 1,12- 1,35); grave HR 1,93 (IC 95% 1,67-2,22). |
|
Weng et al.31 |
2024 |
Meta-análisis de 82 estudios (18 millones pacientes coronarios) |
Prevalencia EPOC 12% (9,9-14,1%) Riesgo ECV OR 0,5 (IC 95% 0,38-0,66); mayor mortalidad hospitalaria OR 1,47 (1,37-1,58); eventos mayores cardiovasculares OR 1,81 (IC 95% 1,44-2,27); ICC OR 2,14 (IC 95% 1,86-2,46); shock cardiogénico OR 1,3 (IC 95% 1,01-1,68); mortalidad a largo plazo OR 1,99 (IC 95% 1,8-2,2) |
|
Nguyen et al.38 |
2016 |
Adultos>65 años entre 2006 y 2012 (73.363 muertes) luego de 3 semanas de infección de influenza en Nueva York |
Mayor muerte cardiovascular +2,3% (IC 95% 0,7-3,9) a +6,3% (IC 95% 3,7-8,9) y mayor muerte por enfermedad coronaria +2,4% (IC 95% 1,1-3,6) a +6,9% (IC 95% 4-9,9%) |
|
Blackburn et al.39 |
2018 |
Estudio retrospectivo de hospitalización post influenza >45 años en Inglaterra entre 2004 y 2015. |
IAM: 1.347 días (RIQ 1.287-1.541) ACV:1.175 días (RIQ 1.023-1.395) |
|
Ohland et al. 40 |
2020 |
Estudio retrospectivo post influenza en Dinamarca entre 2010 y 2016 (n=1350 individuos) |
-Mayor riesgo IAM:1-3 días post: RI 20,1 (RIQ 8,9-45,8, p<0,001); 4-7 días post: RI 11 (RIQ 4,1- 29,8, p<0,001); 8-14 días post: RI 4,9 (RIQ 1,6-15,6, p=0,006) -Mayor riesgo ACV: 1-3 días post: RI 25,5 (RIQ 14,2-45,8, p<0,001); 4-7 días post: RI 3,5 (RIQ 0,9- 1,4, p=0,0079); 8-14 días post: RI 6,3 (RIQ 2,8-14,4, p<0,001) |
Abreviaturas: ACV: Accidente cerebrovascular; ECV: Eventos cardiovasculares; HR: razón de riesgo; IAM: Infarto Agudo de Miocardio; IC 95%: intervalo de confianza 95%; ICC: insuficiencia cardíaca congestiva; OR: razón de momios; RI: rango de incidencia; RIQ: rango intercuartilar 25-75%
5. Infecciones respiratorias e impacto cardio y cerebrovascular
Las infecciones respiratorias agudas son las principales causas de exacerbación de EPOC.5 En la Tabla 2 se resumen los principales mecanismos patogénicos de microrganismos propuestos para generar ECV.11 Dentro del mes del diagnóstico de una exacerbación de EPOC, se observó empeoramiento de ICC, empeoramiento de arritmias y síndrome agudo coronario, IAM o angina inestable.36 El mayor riesgo (90%) ocurrió dentro de los primeros siete días del diagnóstico de una neumonía aguda (NA).36 Un tercio de las complicaciones ocurrieron en pacientes sin antecedentes cardíacos. De las NA que requirieron UTI, casi 50% desarrollaron IAM. La mortalidad de causa cardíaca representó el 27% del total de muertes por NA.36
Son bien reconocidas las complicaciones extrapulmonares de la infección por el virus de la influenza.37Estudios de modelos temporales han encontrado asociación entre epidemias de influenza y mortalidad cardiovascular.38 En pacientes con diagnóstico de influenza, se identificó que las hospitalizaciones por IAM en adultos >45 años fueron 1.347 (RIQ, 1.217–1.541) y 1.175 (RIQ, 1.023–1.395) para ACV.39 En modelos ajustados, todos los virus estuvieron asociados significativamente a hospitalizaciones por IAM y ACV en ≥75 años. Estimaron que 0,4%–5,7% de las hospitalizaciones por IAM y ACV fueron atribuidas a infección respiratoria.39 En otro estudio, se evaluó la incidencia al primer IAM, ajustado a la edad y temporada anual.40 Las infecciones virales (80% influenza) durante una exacerbación de EPOC se asociaron con un riesgo significativamente elevado de IAM de 15,2 (rango de incidencia (RI) 20,1 (rango intercuartilar 25-75%-RIQ- 8,9-45,8, p<0,001), 4,5 (RI 11, RIQ 4,1-29,8, p<0,001) y 4,4 (RI 4,9, RIQ 1,6-15,6, p=0,006) entre los días 1–3, 4–7 y 8–14 días, respectivamente luego de la infección.40 Para ACV, tuvo incidencias de riesgo elevadas (80% por influenza) significativas de 8,3 (RI 25,5 (RIQ 14,2-45,8, p<0,001), 7,8 (RI 3,5 (RIQ 0,9-14,1 p=0,0079) y 6,2 (RI 6,3 (RIQ 2,8-14,4, p<0,001) entre 1–3, 4–7 y 8–14 días posterior a ella.40 La incidencia 21 días previos de influenza estaba relacionada al incremento de 2,3% (IC95% 0,7%–3,9%) a 6,3% (IC95% 3,7%–8,9%) de mortalidad cardiovascular y 2,4% (IC95% 1,1%–3,6%) a 6,9% (IC95% 4%–9,9%) para mortalidad coronaria.38
El virus sincicial respiratorio (VSR) a nivel mundial constituye una de las causas principales de infección respiratoria aguda en niños. La infección por VSR en los adultos >65 años se caracteriza tanto por duplicar sus hospitalizaciones e incremento de mortalidad.37 Los subgrupos A y B del VSR contribuyen sustancialmente a la carga mundial de la infección y/o enfermedad, con similar mortalidad. La inmunosenescencia luego de la quinta década y las comorbilidades constituyen los principales factores de riesgo de mortalidad.41 Se han informado miocarditis, bloqueos cardíacos de segundo grado, taquicardia auricular multifocal y arritmias potencialmente mortales (aleteo auricular con shock cardiogénico, taquicardia ventricular, torsades de pointes y fibrilación ventricular).41,42
Los eventos inflamatorios sistémicos promovidos por la infección del coronoavirus SARS-CoV2 pueden ser agudos o crónicos. Se ha demostrado que el SARS-CoV-2 aumentó la incidencia de miocarditis/pericarditis al menos 15 veces en comparación con los niveles pre-COVID-19, aunque de baja incidencia.43
También al Streptococcus pneumoniae se lo ha vinculado a la patogénesis de las ECV.36 Los mecanismos serían: aumento del tono simpático propio de la infección. Este efecto también lo ocasiona la exposición a la contaminación del aire, en especial por material particulado fino de 2,5 microgramos metro cúbico (PM2.5 µg/m3), aumento de la actividad inflamatoria sistémica, generación de radicales libres y desregulación de la coagulación, promoviendo condiciones protrombóticas y aumento del estrés biomecánico arterial que genera daño endotelial y alteración del balance metabólico en tejidos muy dependientes de oxígeno.36,44 En dos cohortes de adultos sin ECV previa que se hospitalizaron por NA, se determinó mayor riesgo de ECV en los primeros 30 días, declinando al año, pero manteniéndose el riesgo 1,5 veces mayor hasta 10 años.44 Ohland et al. describieron que 35,4% de los IAM y 43,3% de los ACV se asociaron a neumococo, especialmente en las primeras dos semanas posteriores a la infección.40
6.Prevención del impacto cardio-cerebrovascular con intervenciones terapéuticas en EPOC (Tabla 3 B)
A. Cesación tabáquica
Es la intervención más costo-efectiva en la medicina y reduce la mortalidad global, cardiovascular, cerebrovascular y respiratoria (Evidencia A).1,5,45 Nunca debemos dejar de hacer todo lo que esté a nuestro alcance para que el paciente abandone el tabaquismo y que persista el resto de su vida alejado de él, activa o pasivamente.1,5
B.Rehabilitación pulmonar y actividad física
Los niveles de actividad física regulares, moderados y altos ajustados estuvieron asociados con reducción de la mortalidad global creciente (HR 0,76, IC95% 0,65-0,90) y mortalidad respiratoria (HR 0,70, IC95% 0,48-1,02).46 Se determinó que caminar más de 10.000 pasos diarios estuvo asociado a menor riesgo de mortalidad global (media de rango de cambios -MRC, -0,08; IC95%, -0,11 a -0,06), cardiovascular (MRC, -0,1; IC95%, -0,15 a -0,06) y mortalidad por cáncer (MRC, -0,11; IC95% -0,15 a -0,06).47 En rehabilitación respiratoria (ReRe), no hay evidencia que reduzca el riesgo de ECV, aunque sí la mortalidad global, según la antigüedad de los estudios entre 72 a 32%.5 Sin embargo, incluye intervenciones como la cesación tabáquica, educación nutricional, ejercicio y manejo del estrés, que ayudan a reducir riesgos de ECV.5
C. Vacunas
Las vacunas contra el virus de la influenza, virus sincitial respiratorio (VSR) y el neumococo han reducido el riesgo cardiovascular-cerebrovascular de las infecciones que previenen.48-54
Se ha demostrado en adultos >65 años, que la vacunación con influenza redujo la hospitalización por ICC 37% (p=0,04).49 Se asoció a reducción de la mortalidad global entre 39-54% durante tres años.49 La vacunación antigripal, en un estudio ensayo clínico y controlado vs. placebo (n=2571), ha reducido la mortalidad global-IAM-trombosis que justifique stent a 5,3% en el grupo vacunado vs.7,2% control (HR 0,72; IC95% 0,52-0,99; p=0,04) al año.50 La tasa de mortalidad global fue 2,9% en el grupo vacunado vs. 4,9% control (HR 0,59; IC95% 0,39-0,89; p=0,01). La mortalidad cardiovascular fue 2,7% en el grupo vacunado vs. 4,5% control (HR 0,59; IC95% 0,39-0,9; p=0,014). El IAM fue 2% en el grupo vacunado vs. 2,4% control (HR 0,86; IC95% 0,5-1,46, p=0,57).50 En un metaanálisis de Yedlapati et al., en 16 estudios, n=237.058 personas añosas con comorbilidades, la vacunación antigripal se asoció a menor riesgo de mortalidad global (RR: 0,75; IC95%, 0,60–0,93, p=0,01), mortalidad cardiovascular (RR 0,82; IC95% 0,8–0,84, p<0,001), y eventos mayores cardiovasculares (RR 0,87; IC95% 0,8–0,94, p<0,001) vs. control.51 En once temporadas (n=29.178), se determinó una reducción del riesgo cardiovascular de 26% (OR 0,746; IC95% 0,595–0,937).52 Con respecto al VSR, se ha observado con la vacunación bivalente (con la proteína prefusión F, pre-F), reducción de las hospitalizaciones cardiorrespiratorias en 2,9 eventos/1.000 pacientes>60 años/anual (IC95% 0,1-5,71).53 En cuanto a la vacuna antineumocóccica, en un meta-análisis (18 estudios, n=716.108) sobre el efecto protectivo cardiovascular en adultos, se encontró que la vacuna de polisacáridos de 23 antígenos se asoció a menor riesgo cardíaco (RR 0,91, IC95% 0,84-0,99) e IAM (RR 0,88, IC95% 0,79-0,98) en todas las edades, especialmente en >65 años.54 Se asoció a reducción de la mortalidad global (RR 0,78, IC95% 0,68-0,88), especialmente en >65 años (RR 0,71, IC95% 0,6-0,84).54
D. Medicamentos
Existe creciente evidencia del impacto de diferentes fármacos sobre la ECV en la EPOC. El tiotropio demostró (n=5.993 a 4 años) reducción del riesgo de eventos cardíacos (RR 0,84, IC95% 0,73–0,98, p<0,05) como objetivo secundario y reducción de ICC (RR 0,59, IC95% 0,37-0,96, p<0,05).55 El estudio SUMMIT (n=16.485 con factores de riesgo cardiovascular) evaluó el impacto sobre la mortalidad y eventos cardiovasculares mayores de furoato de fluticasona y vilanterol como objetivos primarios compuestos.29 La mortalidad global no fue reducida por la asociación de ambas drogas (p=0,137; HR 0,88; IC95%; 0,74–1,04), o de sus monocomponentes (furoato de fluticasona HR 0,91; IC95%; 0,77–1,08; p=0,284 y vilanterol HR 0,96; IC95%; 0,81–1,14; p=0,655).29
La triple terapia (TT) (LABA/LAMA/GCI) de la asociación de dos broncodilatadores de acción prolongada (agonista β2 adrenérgico y otro anticolinérgico) con un corticoide inhalado está indicada en el grupo GOLD E (pacientes con dos o más exacerbaciones moderadas o una exacerbación grave en el año previo y recuento de eosinófilos ≥300 eosinófilos/μl).5 Ha demostrado reducir las exacerbaciones moderadas y graves, mejorando la función pulmonar y calidad de vida.56-59 En estudios de ensayo clínicos controlados post-análisis del ETHOS e IMPACT, se observó reducción de la mortalidad global por la TT.58-60 En estudios prospectivos y observacionales de vida real, se ha demostrado que la TT cerrada (único dispositivo) reduciría 12% los ECV (HR 0,88; IC95%; 0,83-0,93), y la mortalidad global 18% (HR 0,82; IC95%; 0,19-0,75) comparando la TT (en varios dispositivos), que podría justificarse por mayor adherencia, mejor función pulmonar y reducción de exacerbaciones.61,62
Tabla 3.B.
Impacto de las intervenciones terapéuticas sobre la mortalidad de EPOC e impacto en los eventos cardiovasculares.
|
Autores |
Año |
Diseño |
Resultados |
|---|---|---|---|
|
Cesación tabáquica 5 |
2025 |
Guía basada en la evidencia de actualización anual (GOLD) |
Reduce la mortalidad global HR 1,18 (IC95% 1,02-1,37) |
|
Rehabilitación Respiratoria 5 |
2025 |
Guía basada en la evidencia de actualización anual (GOLD) |
Reducción mortalidad global de estudios antiguos: RR 0,28 (IC 95% 0,1-0,84) Reducción mortalidad global de estudios nuevos: RR 0,68 (IC 95% 0,28-1,67) |
|
García Aymerich et al.46 |
2006 |
Cohorte prospectiva de EPOC, divididos por actividad física baja, moderada y alta (pasos/día) (n=2.386) |
Reducción mortalidad global HR 0,76 (IC 95% 0,65-0,9) Reducción mortalidad respiratoria HR 0,7 (IC 95% 0,48-1,02) |
|
Del Pozo et al.47 |
2022 |
UK Biobank. Cohorte prospectiva seguida a 7 años (n=78.500) Contador de pasos diarios |
Reducción mortalidad global MRC -0,09 (-0,11- - 0,06) Reducción mortalidad cardiovascular MRC -0,1 (-0,15- - 0,06) Reducción mortalidad cáncer MRC -0,11 (-0,15- - 0,06) |
|
Fröbert et al.50 |
2021 |
Personas vacunadas contra influenza vs. control (n=2.571) |
Reducción mortalidad IAM-trombosis con stent HR 0,72 (IC 95% 0,52-0,99, p=0,04) Reducción mortalidad global año HR 0,59 (IC 95% 0,39-0,89, p=0,001) Reducción mortalidad global cardiovascular HR 0,59 (IC 95% 0,39-0,9, p=0,014) Reducción mortalidad IAM HR 0,86 (IC 95% 0,5-1,4, p=NS) |
|
Yedlapati et al.51 |
2021 |
Meta-análisis de 16 estudios (237.058 personas vacunadas contra influenza vs. control) |
Reducción riesgo de mortalidad global (RR: 0,75; IC 95%, 0,60–0,93, p=0,01) Reducción mortalidad cardiovascular (RR 0,82; IC 95% 0,8–0,84, p<0,001) Reducción eventos mayores cardiovasculares (RR 0,87; IC 95% 0,8–0,94, p<0,001) |
|
Huang et al.52 |
2013 |
11 temporadas (n=29.178 pacientes post vacuna contra influenza), |
Reducción riesgo cardiovascular OR 0,74 (IC 5% 0,595-0,937) |
|
Hojjerg et al. 53 |
2025 |
Estudio prospectivo post vacuna proteína de prefusión F de VSR (n=65.642 vacunados vs 65.634 control) |
Reducción riesgo hospitalizaciones por eventos cardiorrespiratorios 2,9/1.000 pacientes >65 años (IC 95% 0,1-5,71) |
|
Marra et al.54 |
2020 |
Meta-análisis de 18 estudios (716.108) personas post-vacuna antineumocócica PPSV23 |
Reducción riesgo cardiovascular RR 0,91 (IC 95% 0,84-0,99) Reducción IAM RR 0,88 (IC 95% 0,79-0,98) |
|
Celli et al.55 |
2012 |
Estudio UPLIFT, prospectivo, controlado, tiotropio vs.tratamiento usual a 4 años (n=5.993 pacientes) |
Reducción del riesgo de eventos cardíacos RR 0,84 (IC 95% 0,73–0,98, p<0,05) como objetivo secundario. Reducción de ICC RR 0,59 (IC 95% 0,37-0,96, p<0,05) como objetivo secundario |
|
Kunisaki et al.29 |
2018 |
Estudio SUMMIT prospectivo, controlado, (n=16.485 con factores de riesgo cardiovascular) evaluó el impacto sobre la mortalidad y eventos cardiovasculares mayores de furoato de fluticasona y vilanterol combinados vs. monoterapias |
No se redujo mortalidad global por la asociación de ambas drogas (HR 0,88 IC 95% 0,74–1,04, p=0,137) No se redujo mortalidad global de sus mono componentes (furoato de fluticasona HR 0,91- IC 95% 0,77–1,08, p=0,284 y vilanterol HR 0,96 IC 95%, 0,81–1,14, p=0,655) |
|
Martinez et al.58 |
2012 |
Estudio ETHOS, prospectivo, controlado, triple terapia vs doble terapia broncodilatadora vs LABA/CI a 1 año (n=8.609 pacientes) |
Reducción de la mortalidad global HR 0,51 (IC 95% 0,33–0,8) como objetivo secundario. |
|
Lipson et al.60 |
2018 |
Estudio IMPACT prospectivo, controlado, controlado, triple terapia vs doble terapia broncodilatadora vs LABA/CI a 1 año (n=10.355 pacientes) |
Reducción de la mortalidad global HR 0,72 (IC 95% 0,53–0,99) como objetivo secundario |
Abreviaturas: CI: corticoides inhalados; HR: razón de riesgo; IAM: infarto agudo de miocardio; ICC: insuficiencia cardíaca congestiva; IC95%: intervalo de confianza 95%; LABA: broncodilatadores beta 2 adrenérgicos de acción prolongada; MRC: media de rango de cambios; OR: razón de momios; PPSV23: vacuna antineumocócica polisacáridos de 23 antígenos; RR: riesgo relativo; VSR: virus sincicial respiratorio.
7. Impacto sobre los costos de una exacerbación de EPOC y más allá
Más allá de los costos directos de la exacerbación por EPOC, ambulatoria u hospitalizada, deberíamos incluir los derivados de las ECV y consecuencias inflamatorias sistémicas de infecciones por influenza, SARS-COV2, VSR y neumococo. Además, deberíamos ponderar los costos indirectos, como son la fragilidad, ausentismo laboral, discapacidad o muerte prematura, que siempre superan varias veces a los costos directos. Los estudios realizados en nuestro país, sólo han evaluado los costos directos de hospitalización por exacerbación de EPOC e influenza, pero se carece de información de los costos derivados de los eventos sistémicos a mediano y largo plazo, e indirectos. Pero también hay que ponderar que, en los países de bajo ingresos y en vías de desarrollo, el impacto es todavía mayor63-66
6.Conclusiones
El consumo de tabaco es la principal causa prevenible de enfermedad respiratoria y ECV, y de muerte prematura.1,2
La mayoría de las referencias citadas en esta revisión en apoyo de la asociación entre EPOC y eventos ECV son estudios de cohortes retrospectivos, registros administrativos o de bases de datos de estudios primarios. Este tipo de evidencia es de bajo nivel de certeza y deberá comprobarse en estudios prospectivos, con mayor tamaño de muestra y el diseño epidemiológico adecuado. Esta revisión narrativa evidencia heterogeneidad en los estudios en la definición de exacerbación, gravedad y desenlaces. Independientemente de su lugar de realización, no se ajustan adecuadamente por variables confundidoras críticas como edad, comorbilidades cardiovasculares previas, estado funcional o adherencia terapéutica, lo que limita la confiabilidad de los resultados.
No obstante, las exacerbaciones de EPOC han dejado de ser un fenómeno restringido al sistema respiratorio. En los últimos años ha crecido la evidencia de ser eventos inflamatorios sistémicos y que aumentarían aún más los riesgos de ECV en las formas más graves. Además, algunos agentes infecciosos virales y bacterianos «per se» generan daños sistémicos adicionales. Probablemente en los próximos años estas enfermedades sindémicas deberán ser abordadas de manera más holística, con una relación más íntima entre el clínico, cardiólogo, neurólogo y neumonólogo.
Las herramientas preventivas de las exacerbaciones de EPOC siguen siendo la cesación tabáquica, la vacunación, la actividad física y la ReRe. La triple terapia reduce la mortalidad en pacientes con EPOC exacerbadores frecuentes (más de dos eventos por año) y fenotipo T2 alto; además, su prescripción en un solo inhalador parecería asociarse con una mejor adherencia.
Esta revisión narrativa tiene como limitación que la elección de la bibliografía citada estuvo vinculada a la subjetividad de los autores, introduciendo sesgos de selección, falta de reproducibilidad, ausencia de una estrategia de búsqueda y criterios de elegibilidad, así como ausencia de evaluación independiente de la selección de los artículos elegidos, que podría afectar las conclusiones alcanzadas.
Futuras investigaciones prospectivas y con desenlaces clínicos validados deberán cuantificar adecuadamente el riesgo cardio-cerebrovascular asociado a las exacerbaciones de EPOC con mayor rigor metodológico.
Financiamiento: los autores declaran que el trabajo no tuvo financiamiento.
Conflicto de intereses: RR: declara no tener conflicto de intereses en el tema. MS: ha participado en programas de educación médica continua para Glaxo SmithKline, AstraZeneca, ELEA, SANOFI, Sequirus y Pfizer. AE: asesor médico externo de Glaxo SmithKline, AstraZeneca, Boehringer Ingelheim. Griphols. Apoyo para concurrencia a congresos de AstraZeneca, Boehringer Ingelheim, ELEA, Novartis, Griphols, Kamada/Tuteur. Programas de educación médica continua para AstraZeneca, Boehringer Ingelheim, ELEA, Novartis, Griphols, Kamada/Tuteur. Investigador Principal de ensayos clínicos de Asma y EPOC patrocinados por Pfizer, Glaxo SmithKline, Boehringer Ingelheim, Pearl,AstraZeneca y Roche/Genetech. MP: ha participado en programas de educación médica continua para Glaxo SmithKline, AstraZeneca, ELEA, SANOFI, Casasco, Knight, Boehringer Ingelheim. Apoyo para concurrencia a congresos de Raffo, BAGO, Tuteur, Montpellier y Cassará. DR: declara no tener conflicto de intereses en el tema.
Contribuciones de los autores: todos los autores contribuyeron de manera equitativa en la revisión de la bibliografía disponible.
Los Editores en Jefe, Dres. Carlos Luna y Francisco Arancibia, realizaron el seguimiento del proceso de revisión y aprobaron este artículo.
Referencias
1. Ministerio de Salud. Guía 2021: Práctica Clínica Nacional de Tratamiento de la Adicción al Tabaco: Recomendaciones basadas en la evidencia. [Internet]. [Consultado 19 abr 2025]. Disponible en: https://www.aamr.org.ar/secciones/tabaquismo_epidemiologia/guia_tabaquismo_2021.pdf
2. World Health Organization. Chronic Obstructive Pulmonary Disease. [Internet]. [Consultado 27 may 2025]. Disponible en: https://www.who.int/news-room/fact-sheets/detail/chronic-obstructive-pulmonary-disease-(copd)
3. Arias S, Echazarreta A. Abordaje del paciente con EPOC. Capítulo 1: Epidemiología de la EPOC. Asociación Argentina de Medicina Respiratoria. Buenos Aires, 2024. pp. 5-20.
4. Echazarreta AL, Arias SJ, Del Olmo R, Giugno ER, Colodenco FD, Arce SC et al. Prevalencia de enfermedad pulmonar obstructiva crónica en 6 aglomerados urbanos de Argentina: el estudio EPOC.AR. Arch Bronconeumol 2018;54:260-9. https://doi.org/10.1016/j.arbres.2017.09.018
5. Global Initiative for Chronic Obstructive Lung Disease. Global Strategy for the Diagnosis, Management and Prevention of COPD 2025. [Internet]. [Consultado 10 mar 2025]. Disponible en: https://goldcopd.org/2025-gold-report/
6. Lawrence H, Hunter A, Murray R, Lim WS, Mckeever T. Cigarette smoking and the currency of infuenza- systematic review. J Infec 2019;79:401-6. https://doi.org/10.1016/j.jinf.2019.08.014ń
7. Han L, Ran J, Ma YW, Suen LKP, Lee PH, Peiris JS et al. Smoking and Influenza-associated morbidity and mortality: a systematic review and meta-analysis. Epidemiology 2019;30:405-17. https://doi.org/10.1097/EDE.0000000000000984
8. Singer M. A dose of drugs, a touch of violance, a case of AIDS: Conceptualizing the SAVA Endemic. Free Inq Creat Sociol 1996;24:99-110.
9. Horton R. Offline: COVID-19 is not a pandemic. Lancet 2020;396:874. https://doi.org/10.1016/S0140-6736(20)32000-6
10. Solidoro P, Albera C, Ribolla F, Bellochia M, Brussino L, Patrucco F. Triple Therapy in COPD: can we welcome the reduction in cardiovascular risk and mortality. Front Med 2022;9:816843. https://doi.org/10.3389/fmed.2022.816843
11. GBD 2015 Mortality and Causes of Death Collaborators. Global, regional, and national life expectancy, all-cause mortality, and cause-specific mortality for 249 causes of death, 1980-2015: a systematic analysis for the Global Burden of Disease Study 2015. Lancet 2016;388:1459–544. https://doi.org/10.1016/S0140-6736(16)31012-1
12. Finkelstein J, Cha E, Scharf SM. Chronic obstructive pulmonary disease as an independent risk factor for cardiovascular morbidity. Int J Chron Obstruct Pulmon Dis 2009;4:337–49. https://doi.org/10.2147/copd.s6400
13. Jimenez J, Sivori M. Comparación de los índices de Charlson y COTE en la EPOC y su relación con la mortalidad. Rev Am Med Respir 2022;1:3-9.
14. MacLeod MA, Knott D, Allinson JPP, Finney LJ, Wiseman DJ, Ritchie AI et al. Prevalence and clinical correlates of radiologically detected coronary artery disease in COPD: a cross-sectional observational study. Am J Respir Crit Care Med 2025;211:946–56. https://doi.org/10.1164/rccm.202404-0838OC
15. Smith MC, Wrobel JP. Epidemiology and clinical impact of major comorbidities in patients with COPD. Int J Chron Obstruct Pulm Dis 2014;9:871–88. https://doi.org/10.2147/COPD.S49621
16. Feary JR, Rodriguez LC, Smith CJ, Hubbard RB, Gibson JE. Prevalence of major comorbidities in subjects with COPD and incidence of myocardial infarction and stroke: a comprehensive analysis using data from primary care. Thorax 2010;65:956–962. https://doi.org/10.1136/thx.2009.128082
17. Izquierdo Alonso JL. EPOC y enfermedad cerebrovascular. Arch Bronconeumol 2010;46:18-22. https://doi.org/
18. Berry CE, Wise RA. Mortality in COPD: Causes, risk factors and prevention. COPD 2010;7:375–82. https://doi.org/10.3109/15412555.2010.510160
19. Mannino DM, Doherty D, Buist AS. GOLD classification of lung disease and mortality: findings from the Arteriosclerosis Risk in Communities (ARIC) study. Respir Med 2006;100:115-22. https://doi.org/10.1016/j.rmed.2005.03.035
20. Soler Cataluña JJ, Martinez Garcia MA, Román Sánchez P, Salcedo E, Navarro M, Ochando R. Severe acute exacerbations and mortality in patients with COPD. Thorax 2005;60:925-31. https://doi.org/10.1136/thx.2005.040527
21. Roversi S, Fabbri LM, Sin DD, Hawkins NM, Agusti A. Chronic obstructive pulmonary disease and cardiac diseases. An urgent need for integrated care. Am J Respir Crit Care Med 2016;194:1319–36. https://doi.org/10.1164/rccm.201604-0690SO
22. Rockwood K, Andrew M, Mitnitski A. An analysis comparing two strategies for the measurement of frailty in elderly individuals. J Gerontol A Biol Sci Med Sci 2007:62A:738-43. https://doi.org/
23. Athanazio RA, Bernal Villada L, Avdeev SN, Wang HC, Ramírez-Venegas A, Sívori M et al. Rate of severe exacerbations, healthcare resource utilization and clinical outcomes in patients with COPD in low-income and middle countries: results from the EXACOS International Study. BMJ Open Respir Res 2024:11:e002101. https://doi.org/10.1136/bmjresp-2023-002101
24. Aisanov Z, Khaltaev N. Management of cardiovascular comorbidities in COPD patients. J Thorac Dis 2020;12:2791–802. https://doi.org/10.21037/jtd.2020.03.60
25. Donaldson GC, Hurst JR, Smith CJ, Hubbard RB, Wedzicha JA. Increased risk of myocardial infarction and stroke following exacerbation of COPD. Chest 2010;137:1091–7. https://doi.org/10.1378/chest.09-2029
26. Rothnie K, Müllerova H, Smeeth L, Quint JK. Natural History of COPD exacerbations in a general practice-based population with COPD. Am J Respir Crit Care Med 2018;198:464–71. https://doi.org/10.1164/rccm.201710-2029OC
27. Whittaker H, Rubino A, Müllerova H, Morris T, Varghese P, Xu Y et al. Frequency and severity of exacerbations of COPD associated with future ris of exacerbations and mortality: A UK Routine Health Care Data Study. Int J COPD 2022:17 427–37. https://doi.org/10.2147/copd.s346591
28. Vanflateren LE, Lindberg A, Zhou C, Nyberg F, Stridsman C. Exacerbation risk and mortality in GOLD Group A and B patients with and without exacerbation history. Am J Respir Crit Care Med 2023;208;163-75. https://doi.org/10.1164/rccm.202209-1774OC
29. Kunisaki KM, Dransfield MT, Anderson JA, Brook RD, Calverley PMA, Celli BR et al. Exacerbations of COPD and cardiac events: a post hoc cohort analysis from the SUMMIT randomized clinical trial. Am J Respir Crit Care Med 2018;198:51–7. https://doi.org/10.1164/rccm.201711-2239OC
30. Daniels K, Lanes S, Tave A, Pollack MF, Mannino DM, Criner G et al. Risk of death and cardiovascular events following an exacerbation of COPD: The EXACOS-CV. Int J COPD 2024;19:225-41. https://doi.org/10.2147/COPD.S438893
31. Weng K, Zhang X, Liu W, Xu Z, Xie B, Dai H. Prevalence and impact of CPD in ischemic heart disease: a systematic review and meta-analysis of 18 million patients. Int JCOPD 2024; 1:2333-45. https://doi.org/10.2147/COPD.S474223
32. Pirera E, Di Raimondo D, D’Anna L, Tuttolomondo A. Risk trajectory of cardiovascular events after an exacerbation of chronic obstructive pulmonary disease: A systematic review and meta-analysis. Eur J Intern Med 2025;135:74-82. https://doi.org/
33. Shrikrishna D, Steer J, Bostock B, Dickinson SW, Piwko A, Ramalingam S et al. Chronic Obstructive Pulmonary Disease and the Management of Cardiopulmonary Risk in the UK: A Systematic Literature Review and Modified Delphi Study. Int J Chron Obstruct Pulmon Dis 2025;20:2073-2090. https://doi.org/
34. Kostikas K, Gogali A, Hillas G. Cardiovascular disease and COPD: adding a third dimension to the ABE global Initiative for Chronic Obstructive Pulmonary Disease 2023 Chronic Obstructive Pulmonary Classification. Am J Crit Care Respir Med 2023;208:502-4. https://doi.org/10.1164/rccm.202304-0691LE
35. Gedebjerg A, Szepligeti SK, Holm Wackerhausen LM, Horváth-Puhó E, Dahl R, Hansen JG et al. Prediction of mortality in patients with COPD with the new Global Initiative for Chronic Obstructive Lung Disease 2017 classification: a cohort study. Lancet Respir Med 2018;6:204-12. https://doi.org/10.1016/S2213-2600(18)30002-X
36. Corrales Medina VF, Musher DM, Shachkina S, Chirinos JA. Acute neumonia and the cardiovascular system. Lancet 2013;381:496-505. https://doi.org/10.1016/S0140-6736(12)61266-5
37. Nowalk M, D’Agostino H, Dauer K, Stiegler M, Zimmerman RK, Balasubramani GK et al. Estimating the burden of adult hospitalized RSV infection including special populations. Vaccine 2022;40:4121–27. https://doi.org/10.1016/j.vaccine.2022.05.077
38. Nguyen JL, Yang W, Ito K, Matte TD, Shaman J, Kinney PL. Seasonal influenza infections and cardiovascular disease mortality. JAMA Cardiol 2016;1:274–81. https://doi.org/10.1001/jamacardio.2016.0433
39. Blackburn R, Zhao H, Pebody R, Hayward A, Warren-Gash C. Laboratory-confirmed respiratory infections as predictors of hospital admission for myocardial infarction and stroke: time series analysis of english data for 2004-2015. Clin Inf Dis 2018;67:9-17. https://doi.org/10.1093/cid/cix1144
40. Ohland J, Warren-Gash C, Blackburn R, Molbak K, Valentiner-Branth P, Nielsen J et al. Acute myocardial infarctions and stroke triggered by laboratory-confirmed respiratory infections in Denmark, 2010-2016. Eur Surveill 2020;25:1900199. https://doi.org/10.2807/1560-7917.ES.2020.25.17.1900199
41. GBD 2016 Lower Respiratory Infections Collaborators. Estimates of the global, regional, and national morbidity, mortality, and etiologies of lower respiratory infections in 195 countries, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet Infect Dis 2018;18:1191–210. https://doi.org/10.1016/S1473-3099(18)30310-4
42. Li Y, Kulkarni D, Begier E, Wahi-Singh P, Wahi-Singh B, Gessner B et al. Adjusting for case under-ascertainment in estimating RSV hospitalization burden of older adults in high-income countries: a systematic review and modeling study. Infect Dis Ther 2023;12:1137–49. https://doi.org/10.1007/s40121-023-00792-3
43. Fairweather DL, Beetler DJ, Di Florio DN, Music N, Heidecker B, Cooper Jr LT. COVID-1, myocarditis and pericarditis. Circulation Research 2023;132:1302–19. https://doi.org/10.1161/CIRCRESAHA.123.321878
44. Corrales-Medina VF, Alvarez KN, Weissfeld LA, Angus DC, Chirinos JA, Chang CCH et al. Association Between Hospitalization for Pneumonia and Subsequent Risk of Cardiovascular Disease. JAMA 2015;313:264–74. https://doi.org/10.1001/jama.2014.18229
45. Huimin T, Zheng T, Jingchun H, Dajun L, Zhijun Z, Yuan L et al. A Scoping Review of Factors Influencing Smoking Cessation in Patients with Chronic Obstructive Pulmonary Disease. COPD 2024;21:2390988. https://doi.org/10.1080/15412555.2024.2390988
46. Garcia Aymerich J, Lange P, Benet M, Schnohr P, Antó JM. Regular physical activity reduces hospital admission and mortality in COPD: a population based cohort study. Thorax 2006;61:772-8. https://doi.org/10.1136/thx.2006.060145
47. Del Pozo Cruz B, Ahmadi MN, Lee IM, Stamatakis E. Prospective associations of daily step counts and intensity with cancer and cardiovascular disease incidence and mortality and all-cause mortality. JAMA Inter Med 2022;182:1139-48. https://doi.org/
48.Clarc C, Oseni Z, Flowers N, Kshtkar-Jahromi M, Rees K. Influenza vaccines for preventing cardiovascular disease. Cochrane Database Sys Rev 2015;5:CD005050. https://doi.org/10.1002/14651858.CD005050.pub3
49. Nichol KL, Margolis KL, Wuorenma J, Von Sternberg T. The efficacy and cost-effectiveness of vaccination against influenza among elderly persons living in the community. New Engl J Med 1994;331:778-84.
50. Fröbert O, Götberg M, Erlinge D, Akhtar Z, Christiensen EH, Maclntyre CR et al. Influenza vaccination after myocardial infarction: a randomized, double-blind, placebo-contrplled, multicenter trial. Circulation 2021;144:1476-84. https://doi.org/10.1161/CIRCULATIONAHA.121.057042
51. Yedlapati SH, Khan SU, Talluri S, Lone AN, Khan MZ, Khan MS et al. Effects of influenza vaccines on mortality and cardiovascular outcomes in patients with cardiovascular disease: a systematic review and meta-analysis. J Am Heart Assoc 2021;10:e19636. https://doi.org/10.1161/JAHA.120.019636
52. Huang CL, Nguyen PA, Kuo PL, Hsu YH, Jian WS. Influenza vaccination and reduction in risk of ischemic heart disease among COPD elderly. Comp Meth Prog Biomd 2013;111:507-11. https://doi.org/10.1016/j.cmpb.2013.05.006
53. Hojbjerg Lassen MC, Johansen ND, Christensen S, Aliabadi N, Skaarup KG, Modin D et al. Bivalente RSV prefusion F protein-based vaccine for preventing cardiovascular ospitalizations in older adults: a prespecified analysis of the DAN-RSV trial. JAMA 2025;e2515405 https://doi.org/
54. Marra F, Zhang A, Gillman E, Bessai K, Parhar K, Vadlamudi NM. The protective effect of pneumococcal vaccination on cardiovascular disease in adults: a systematic review and meta-analysis. Int J Inf Dis 2020;99:204-13. https://doi.org/10.1016/j.ijid.2020.07.038
55. Celli B, Decramer M, Kesten S, Liu D, Mehra S, Tashkin DP. Mortality in the 4-year trial of tiotropium (UPLIFT) in patients with COPD. Am J Respir Crit Care Med 2012;180:948-55. https://doi.org/10.1164/rccm.200906-0876OC
56. Lipson DA, Barbhart F, Brealey N, Brooks J, Criner GJ, Day NC et al. Once-daily single-inhaler triple versus dual therapy in patients with COPD. New Engl J Med 2018;378:1671-80. https://doi.org/10.1056/NEJMoa1713901
57. Rabe K, Martinez F, Ferguson GT, Wang C, Singh D, Wedzicha JA et al. Triple therapy at two glucocorticoid doses in moderate to very severe COPD. New Engl J Med 2020;383:35-48. https://doi.org/10.1056/NEJMoa1916046
58. Martinez F, Rabe K, Ferguson GT, Wedzicha JA, Singh D, Wang C et al. Reduced all-cause mortality in the ETHOS trial of Budesonide/Glycopyrrolate/Formoterol for COPD: a randomzied, double blind, multicenter, parallel-group study. Am J Respir Crit Care Med 2021;203:553–64. https://doi.org/10.1164/rccm.202006-2618OC
59. Rogliani P, Manzetti GM, Cazzola M, Calzetta L. Real-World Effectiveness of Triple Extrafine Fixed-Dose Combination with Beclomethasone/Formoterol/Glycopyrronium on Symptoms and Lung Function in COPD: A Systematic Review and Meta-Analysis. Int J Chron Obstruct Pulmon Dis 2025; 20:1723-36. https://doi.org/
60. Lipson DA, Crim C, Criner GJ, Day NC, Dransfield MT, Halpin D et al. Reduction in all-cause mortality wit fluticasone furoate/Umeclidinium/Vilanterol in patients with COPD. Am J Respir Crit Care Med 2020;201:1508–16. https://doi.org/10.1164/rccm.201911-2207OC
61. Halpin DMG, Worsley S, Ismaila AS, Beeh M, Midwiner D, Kocks JWH et al. INTREPID: single-versus multiple inhaler triple therapy for COPD in usual clinical practice. ERJ Open Res 2021;7:00950-2020. https://doi.org/10.1183/23120541.00950-2020
62. Pollack M, Rapsomaniki E, Anzueto A, Rhodes K, Hawins NM, Volgelmeier CF et al. Effectiveness of Single Versus Multiple Inhaler Triple Therapy on Mortality and Cardiopulmonary Risk Reduction in COPD: The SKOPOS-MAZI Study. Am J Med 2025;138:650-9. https://doi.org/10.1016/j.amjmed.2024.11.007
63. Pascansky D, Sivori M, Capelli L. EPOC reagudizada hospitalizada: Estudio de costos directos en un hospital público de la Ciudad de Buenos Aires. Rev Am Med Respir 2022;22:299-308. https://doi.org/10.56538/ramr.LYBB1788
64. Sivori M, Pascansky D, González L, Mancuso M. Neumonía por virus de la influenza: Estudio de costos en un hospital público de la ciudad de Buenos Aires. Rev Am Med Resp 2024;24:160-7. https://doi.org/10.56538/ramr.nv96-q7av
65. Vlachaki I, Donhauser S, Wise RA, Chen Y, Madoni A, Argentina S et al. A Systematic Literature Review of the Humanistic, Economic, Sociodemographic, and Environmental Burden Associated with Severe COPD. Int J Chron Obstruct Pulmon Dis 2025;20:2493-2523. https://doi.org/10.2147/COPD.S510623
66. Adhikari S, Thapa S, Rattanapan C, Laosee O, Sriram S, Bhatta J et al. Evaluating the impact of self-management interventions on COPD outcomes in low- and middle-income countries in Asia: a systematic review. Health Qual Life Outcomes 2025;23:81. https://doi.org/10.1186/s12955-025-02382-y