
Artículo Original | Respirar, 2026; 18 (1): 124-148 | ISSN 2953-3414 | https://doi.org/10.55720/respirar.18.1.10
Registro latinoamericano de pacientes con Enfermedad Pulmonar Post-Tuberculosis: análisis de las condiciones clínicas, función pulmonar, calidad de vida y rehabilitación. Estudio multicéntrico
Latin American Registry of patients with Post-Tuberculosis Lung Disease: Analysis of clinical conditions, pulmonary function, quality of life, and rehabilitation. Multicenter Study
Colaboradores: miembros del Departamento de Tuberculosis ALAT.
1 Universidad de Buenos Aires, Instituto de Tisioneumonología Prof. Dr. Raúl Vaccarezza, Buenos Aires, Argentina. 2 Ministerio de Salud de la Nación Argentina, Comité asesor del Programa Nacional de Tuberculosis, Argentina. 3 Clínica Privada Monte Grande, Buenos Aires, Argentina. 4 Global Tuberculosis Network (GTN). 5 WHO Collaborating Centre for TB and Lung Disease, Maugeri Care and Research Institute, Tradate, Italia. 6 Istituti Clinici Scientifici Maugeri IRCCS, Tradate, Italia. 7 Pulmonary Health Center, Ciudad Juárez Chihuahua, México. 8 Hospital de Infecciosas Francisco Javier Muñiz, Ciudad de Buenos Aires, Argentina. 9 Sanatorio Güemes, Ciudad de Buenos Aires, Argentina. 10 Servicio de Salud Metropolitano Central, Programa de Tuberculosis, Santiago, Chile. 11 Instituto Nacional Cardiopulmonar, Servicio de Neumología, Tegucigalpa, Honduras. 12 Servicio de Salud Metropolitano Central, Programa de Tuberculosis pediátrico, Santiago, Chile. 13 Hospital de Infectología “Dr. José Daniel Rodríguez Maridueña”, Servicio de Infectología/ Tuberculosis, Guayaquil, Ecuador. 14 Clínica Internacional y Hospital Nacional Arzobispo Loayza, Servicio de Neumología, Lima, Perú. 15 Ministerio de Salud del Perú, Hospital San José del Callao, Comité de Evaluación de Retratamientos TB MDR Diresa Callao, Comité Nacional de Evaluación de Retratamientos, Perú. 16 Universidad Ricardo Palma, Facultad de Medicina, Instituto de Investigaciones en Ciencias Biomédicas (INICIB), Lima, Perú. 17 Hospital Nacional Dos de Mayo, Servicio de Neumología, Lima, PerúAutor corresponsal:
Sandra Janete Inwentarz. E-mail: sandra@inwentarz.com.ar | tuberculosis@alatorax.org
Recibido:
29 julio 2025
Aprobado:
07 noviembre 2025
Resumen
Introducción: La tuberculosis (TB) es una enfermedad transmisible incluida en la Iniciativa de la Organización Panamericana de la Salud para la Eliminación de Enfermedades en las Américas. En América Latina, se ha reportado un aumento sostenido de la TB en los últimos años. Paralelamente, se ha reconocido la Enfermedad Pulmonar Post-Tuberculosis (EPPT) como una entidad clínica relevante, asociada a secuelas respiratorias, funcionales y psicosociales que impactan negativamente en la calidad de vida y generan elevados costos catastróficos en salud. Sin embargo, la magnitud de la EPPT y sus características clínicas en América Latina aún no se encuentran claramente definidas.
Objetivo: Describir las características demográficas, clínicas, funcionales, radiológicas y de calidad de vida de pacientes con EPPT en América Latina, utilizando un registro estandarizado, con el fin de generar evidencia que permita orientar recomendaciones para su diagnóstico y manejo oportuno.
Metodología: Registro multicéntrico, utilizando un modelo estandarizado de historia clínica compartida, disponible en la plataforma REDCap de la Asociación Latinoamericana de Tórax (ALAT). Se recopilarán datos clínicos relevantes, estudios funcionales respiratorios, imágenes radiológicas, evaluación de calidad de vida y el uso e impacto de la rehabilitación respiratoria en pacientes con EPPT provenientes de distintos países de América Latina.
Conclusiones: Este registro permitirá estimar la carga de la EPPT en América Latina y caracterizar integralmente a los pacientes afectados. La información obtenida contribuirá a fortalecer las estrategias de diagnóstico, tratamiento y rehabilitación, promoviendo un enfoque integral orientado a reducir la discapacidad y los costos catastróficos asociados a esta condición.
Palabras clave: enfermedad pulmonar post-tuberculosis; tuberculosis enfermedad; secuelas post tuberculosis; rehabilitación pulmonar; complicaciones post tuberculosis.
Abstract
Introduction: Tuberculosis (TB) is a communicable disease included in the Pan American Health Organization’s Initiative for the Elimination of Diseases in the Americas. In Latin America, unlike other regions, the World Health Organization has reported a sustained increase in TB incidence in recent years. In parallel, Post-Tuberculosis Pulmonary Disease (PTPD) has emerged as a relevant clinical entity, associated with respiratory, functional, and psychosocial sequelae that negatively impact quality of life and generate substantial catastrophic health costs. However, the burden and clinical characteristics of PTPD in Latin America remain poorly defined.
Objective: To describe the demographic, clinical, functional, radiological, and quality-of-life characteristics of patients with PTPD in Latin America through a standardized registry, in order to generate evidence to support recommendations for timely diagnosis and management in the region.
Methods: A multicenter registry was developed using a standardized shared medical record model available on the REDCap (Research Electronic Data Capture) platform of the Asociación Latinoamericana de Tórax (ALAT). Relevant clinical data, pulmonary function tests, radiological imaging, quality-of-life assessments, and the use and impact of pulmonary rehabilitation will be collected from patients with PTPD across participating Latin American countries.
Conclusions: This registry will allow estimation of the burden of PTPD in Latin America and provide a comprehensive characterization of affected patients. The generated data will support strategies aimed at improving diagnosis, treatment, and rehabilitation, promoting an integrated approach to reduce disability and catastrophic health costs associated with this condition.
Keywords: post-tuberculosis lung disease; tuberculosis disease; post-tuberculosis sequelae; pulmonary rehabilitation; post-tuberculosis complications.
Introducción
a) Contexto general y relevancia de la tuberculosis en la región:
La tuberculosis (TB) continúa siendo un grave problema de salud pública a pesar de ser una enfermedad prevenible y curable. La mayoría de las personas que la contraen son adolescentes y adultos jóvenes con alta carga bacilar, en consecuencia, alta probabilidad de diseminación de la enfermedad.
La eliminación de la TB para el año 2030 es uno de los objetivos de desarrollo sostenible (ODS) propuesto por la Organización Mundial de la Salud (OMS). La TB es una de las 30 enfermedades transmisibles contempladas dentro de la Iniciativa de la Organización Panamericana de la Salud (OPS), para la Eliminación de Enfermedades en las Américas, región que ya presenta éxitos previos en la consecución de la eliminación de diferentes enfermedades, no así con la TB.
Los esfuerzos de la lucha contra la TB se centran habitualmente en un diagnóstico precoz, y un tratamiento eficaz y oportuno para romper la cadena de transmisión de Mycobacterium tuberculosis. Sin embargo, en los últimos años, a posteriori de la asociación sindémica TB/COVID-19, han aparecido cada vez más evidencias sobre las graves secuelas clínicas, funcionales y psicosociales que puede ocasionar la TB, condición que se ha definido como Enfermedad Pulmonar Post-Tuberculosis (EPPT).1 Esto genera un desafío adicional a las consecuencias físicas y psicosociales negativas, sumado al estigma con el que cargan nuestros pacientes.2-3
Se estima que más de la mitad de los pacientes que completan tratamiento de TB presentan secuelas de diversa magnitud, con un amplio espectro de manifestaciones.4,5,6 Estas incluyen síntomas respiratorios persistentes con exacerbaciones episódicas, insuficiencia respiratoria crónica, trastornos emocionales y desafíos psicosociales que afectan negativamente la calidad de vida y generan un alto costo catastrófico relacionado con la salud, superior al 20% de los ingresos anuales del hogar.7
b) Definición y desafíos de la Enfermedad Pulmonar Post Tuberculosis (EPPT):
La EPPT se definió durante el primer Simposio Internacional sobre Enfermedad Post-TB, celebrado en Stellenbosch, Sudáfrica, en el año 2019, como: “Evidencia de anomalía respiratoria crónica, con o sin síntomas, atribuible, al menos en parte a tuberculosis pulmonar previa”.1,3
Para apoyar el abordaje clínico de los pacientes con EPPT, en 2021 se publicaron unos estándares clínicos mínimos para el diagnóstico, tratamiento y rehabilitación de esta patología.3,8
La EPPT sigue siendo infradiagnosticada y escasamente abordada,9-12 a pesar de que la tuberculosis afecta anualmente a casi 11 millones de personas, niños, adolescentes y adultos en todo el mundo,12-14 y a pesar de que en los últimos 15-20 años, se observa el deterioro que presentan algunos pacientes, luego de haber finalizado correctamente el tratamiento.15-19 El segundo Simposio Internacional sobre sobre esta condición en Stellenbosch, Sudáfrica, que tuvo lugar en abril de 2023, contó con la asistencia de médicos expertos, investigadores, financiadores, sobrevivientes y responsables políticos de más de 30 países, que pidieron una mayor concientización, promoción, investigación y acción para esta importante enfermedad crónica.
Con el enfoque reciente de incluir bajo el término EPOC cualquier condición causante de obstrucción crónica al flujo de aire, la EPPT puede considerarse como un factor de riesgo para la EPOC o constituirse efectivamente en un subtipo de EPOC.4 Según las guías GOLD 2025, 23 estudios fueron analizados y se obtuvo una odds ratio 2,59 (IC del 95%) con una prevalencia agrupada de EPOC en pacientes con tuberculosis pulmonar previa del 21% (IC del 95 %: 16-25%). En este sentido, la TB sería a la vez un diagnóstico diferencial de la EPOC y una comorbilidad potencial.4,5
Es necesario destacar que se conoce muy poco sobre el comportamiento de la enfermedad obstructiva16,20-22 relacionada con secuelas de TB: el curso clínico, la ocurrencia de exacerbaciones, la trayectoria de la función pulmonar y su tratamiento. Dado que se trata de una condición de etiología bien conocida, es recomendable referirse a secuelas de TB o EPPT con obstrucción al flujo de aire más que a EPOC por TB, si bien las guías GOLD 2023-2024-2025 reconocen la TB pulmonar previa como una causa reconocida de daño estructural permanente en el pulmón, incluyendo bronquiectasias, fibrosis, enfisema localizado y obstrucción de las vías aéreas. Este daño puede provocar una limitación persistente al flujo aéreo, que cumple criterios espirométricos de EPOC, aunque el paciente nunca haya fumado.5
Sin embargo, GOLD aclara que estos pacientes a menudo no encajan perfectamente en las definiciones clásicas de EPOC y, por eso, se recomienda un enfoque individualizado.
Las guías GOLD introducen el concepto de “etiotipos” de EPOC, reconociendo que la enfermedad puede tener diversas causas, incluyendo infecciones como la tuberculosis. En este contexto, se menciona que la tuberculosis puede causar EPOC, lo que implica que otras infecciones crónicas también podrían llevar a esta condición.
c) Justificación: Justificación del estudio según el método FINER
1. Factibilidad
- La implementación del registro latinoamericano de enfermedad pulmonar post tuberculosis (EPPT) es viable ya que se basa en la recopilación de datos clínicos a través de una historia clínica estandarizada en una plataforma REDCap, una herramienta ampliamente utilizada en investigaciones multicéntricas.23
- Existen antecedentes y guías que respaldan la necesidad de este estudio, como las Recomendaciones para el manejo de la enfermedad pulmonar post tuberculosis de la Asociación Latinoamericana de Tórax (ALAT), lo que proporciona un marco conceptual sólido.8,23
- La colaboración internacional entre distintos países latinoamericanos permitirá fortalecer la recolección de datos y facilitará la adaptación de estrategias según los recursos y particularidades de cada sistema de salud.
- La viabilidad técnica y logística se apoya en la participación de profesionales de distintos centros y la utilización de tecnologías digitales para la recopilación y análisis de información.
2. Interesante
- La tuberculosis es una de las principales enfermedades infecciosas a nivel mundial, pero su impacto a largo plazo en la función pulmonar ha sido menos estudiado, especialmente en América Latina.
- La falta de un registro unificado impide conocer la verdadera carga de la EPPT en la región, lo que dificulta el diseño de estrategias de diagnóstico, manejo y rehabilitación.
- El estudio responde a la necesidad de una atención integral centrada en la persona, promovida por la Organización Mundial de la Salud (OMS), que abarca tanto la fase infecciosa aguda como sus consecuencias crónicas. 8,24-26
- Contar con información específica permitirá concientizar a los profesionales de la salud y a los tomadores de decisiones sobre la importancia de la EPPT, impulsando cambios en la práctica clínica y en las políticas públicas. 3,4,8
3. Novedoso
- Actualmente, no existen registros epidemiológicos unificados sobre EPPT en América Latina, por lo que este estudio representa una iniciativa pionera en la región.
- El desarrollo de una historia clínica integral y estandarizada permitirá obtener datos comparables entre distintos países y facilitará futuras investigaciones.
- La recolección de datos contribuirá a caracterizar mejor la enfermedad, identificando factores de riesgo, evolución clínica, impacto en la calidad de vida y respuesta a diferentes estrategias terapéuticas.
- La información obtenida permitirá diseñar estrategias personalizadas y basadas en evidencia, favoreciendo el desarrollo de programas de rehabilitación pulmonar y seguimiento a largo plazo adaptados a la realidad de cada país. 27-30
4. Ético
- La recopilación de datos será realizada con plataformas seguras (REDCap), garantizando la confidencialidad y protección de la información de los pacientes, en cumplimiento con regulaciones internacionales de privacidad de datos.
- Se asegurará el consentimiento informado de los pacientes, en los centros que así lo requieran (no obligatorio para este tipo de estudio), respetando sus derechos y asegurando que comprendan la finalidad del estudio y su impacto en la mejora de la atención.
- El estudio busca mejorar la calidad de vida de los pacientes y reducir desigualdades en el acceso a la atención médica, lo que se alinea con los principios de justicia y equidad en salud.
- Los resultados permitirán implementar estrategias que eviten la discriminación y exclusión social que sufren muchos pacientes post tuberculosis debido a secuelas respiratorias y estigmatización.
5. Relevante
- La EPPT genera una carga significativa en términos de discapacidad, costos económicos y calidad de vida, afectando a personas en edad productiva y agravando la pobreza en comunidades vulnerables.
- Un manejo inadecuado de la EPPT puede llevar a mayor morbilidad, necesidad de hospitalizaciones recurrentes y sobrecarga de los sistemas de salud, por lo que contar con estrategias efectivas de diagnóstico y tratamiento es esencial.9
- La creación de un registro único latinoamericano permitirá obtener datos epidemiológicos precisos que orienten futuras políticas de salud pública y asignación de recursos.
- Los hallazgos del estudio podrán ser utilizados para desarrollar guías clínicas actualizadas, y mejorar la detección temprana y acceso a tratamientos de rehabilitación pulmonar en la región.
- Este estudio sentará las bases para futuras investigaciones sobre biomarcadores, tratamientos innovadores y estrategias de prevención de secuelas pulmonares, fortaleciendo la capacidad de respuesta en América Latina.
Objetivos
a) Objetivo general:
- Determinar la prevalencia de EPPT en los países participantes.
- Describir las características demográficas, clínicas, funcionales, radiológicas y de calidad de vida de estos pacientes con EPPT.
b) Objetivos específicos:
- Conocer las características clínicas, funcionales y radiológicas más frecuentes de los pacientes con EPPT.
- Conocer el grado de severidad de los pacientes con EPPT.
- Correlacionar estas variables con la evolución de la EPPT.
- Evaluar el impacto de la EPPT en la calidad de vida.
- Determinar la proporción de pacientes con EPPT que podrían beneficiarse con un programa de rehabilitación pulmonar. 40-43
- Proponer lineamientos preliminares para el seguimiento y abordaje integral de pacientes con EPPT en contextos de alta y moderada carga de TB.
Metodología
a) Diseño del estudio:
Es un estudio descriptivo, multicéntrico, observacional, de cohorte, basado en el uso de la plataforma REDcap (Research Electronic Data Capture), para la recolección y análisis de datos clínicos, imagenológicos, funcionales y de calidad de vida en pacientes con EPPT en los países participantes.23
b) Fortalezas metodológicas:
- Estudio multicéntrico: Permite incluir una muestra diversa y representativa de distintos contextos latinoamericanos. Uso de la plataforma REDCap: garantiza la estandarización, trazabilidad y calidad de los datos recolectados.
- Enfoque integral: Combina datos clínicos, funcionales, imagenológicos y psicosociales para un análisis multidimensional de la EPPT. Los datos evaluados en los pacientes, tanto los funcionales como el cuestionario de calidad de vida, se recolectarán al inicio del estudio, al 6 mes y a los 12 meses.
c) Instrumentos de recolección de datos:
Se utilizará el modelo de historia clínica única (Anexo 1), utilizando estándares internacionales de diagnóstico, tratamiento y rehabilitación, que estará disponible en la plataforma REDCap de ALAT. La REDCap, ampliamente usada en la comunidad académica, es un software de captura de datos electrónicos y una metodología de flujo de trabajo para diseñar bases de datos de investigación de ensayos clínicos e investigación traslacional. Se caracteriza por operar en navegadores web y desarrollarse con base en la investigación de metadatos.
El software REDCap intenta proporcionar soporte informático para investigadores clínicos y fomentar una red colaborativa de investigadores institucionales que compartan y apoyen a REDCap como una herramienta de investigación común. Es una red internacional colaborativa de casi 2.500 instituciones socias en 115 países, con más de 590.000 usuarios finales usando el software en más de 450.000 proyectos de investigación.23
La historia clínica única incluye datos demográficos, antecedentes médicos, evaluación funcional pulmonar, imagenológicas y de calidad de vida relacionada con la salud y aspectos psicosociales.
La calidad de vida será evaluada mediante un instrumento estandarizado, el Cuestionario de Enfermedades Respiratorias Crónicas (CRQ), que evalúa el componente disnea, actividad y bienestar emocional; este cuestionario ha sido implementado tanto en niños y adultos, y resulta conveniente para este estudio. Se seleccionarán coordinadores regionales en los diferentes países para el ingreso de los datos de cada paciente. Estos recibirán una capacitación en el uso de REDcap impartida por ALAT.38,39
d) Población y muestra:
Pacientes que, habiendo finalizado el tratamiento de TB pulmonar, presenten alguna evidencia clínica, imagenológica y/o funcional de secuelas pulmonares por TB.
1) Criterios de inclusión
- Pacientes de todos los grupos etarios (incluidos niñas, niños y adolescentes) con antecedente de tuberculosis (TB) confirmada por criterios clínicos, radiológicos, bacteriológicos y/o anatomopatológicos; que hayan cumplido con algún criterio de curación clínico, radiológicos y/o bacteriológico y se encuentren registrados en los sistemas de notificación de enfermedad en los dos años previos a la encuesta de EPPT; y que al momento de la evaluación presenten manifestaciones clínicas, radiológicas y/o funcionales compatibles con EPPT.8,31,32
- Es requisito obligatorio para el registro en la REDcap la valoración de las siguientes características, según edad:
- Signo-sintomatología de enfermedad post tuberculosis,
- Examen físico completo,
- Score de calidad de vida (CV),31,33
- Valoración imagenológica, al menos radiológica,
- Valoración de la función pulmonar, al menos espirometría,
- Test de caminata de 6 min,
- Saturometría.
- El resto de las variables son opcionales y se cargarán según disponibilidad en el anexo de la historia clínica y en la REDcap.
2) Criterios de exclusión
- Pacientes con otras enfermedades respiratorias crónicas, no relacionadas con TB, que presenten cambios estructurales y funcionales asociados. Por ejemplo, pacientes en seguimiento por otras patologías respiratorias que en el transcurso de su seguimiento presentan tuberculosis pulmonar.
- Pacientes que presenten como comorbilidad enfermedades cardiovasculares con alteración de la clase funcional.
- Casos de TB pulmonar activa o en tratamiento inicial al momento del estudio.
3) Variables de estudio:
- Características demográficas: sexo, edad, nivel socioeconómico, nivel educativo, cobertura y/o seguro médico, lugar de residencia (ciudad y país), país de origen/nacionalidad (país).
- Historia de TB: número de episodios, fecha de fin de último episodio, fecha de diagnóstico de primer episodio, tiempo de enfermedad previo a diagnóstico de primer episodio, localización de la TB, tipo de susceptibilidad de la TB inicial, aparición de resistencia, duración del último tratamiento, tipo de tratamiento, carga microbiológica inicial, regularidad del tratamiento, tipo de administración del tratamiento, pérdida de seguimiento, historia y severidad de reacciones adversas.
- Comorbilidades: diabetes mellitus, VIH/SIDA, asma/hiperreactividad bronquial, neoplasias malignas sólidas o hematológicas, enfermedades autoinmunes y/o inmunosupresoras, medicación inmunosupresora.
- Exposiciones ambientales/laborales y hábitos nocivos. Ocupación, hobbies, características de la vivienda, urbana o rural. Hábitos nocivos: tabaco, alcohol, drogas (inhaladas, inyectables).
- Estado clínico actual: signos y síntomas respiratorios, síntomas sistémicos, exacerbaciones respiratorias, hospitalizaciones post TB, medicación habitual para enfermedad respiratoria, uso crónico de oxígeno.
- Características funcionales:
- Espirometría: Capacidad Vital Forzada (FVC), Volumen Espiratorio Forzado en el primer segundo (FEV1), Flujos Medios forzados (FMF 25/75%).
- Capacidad de Difusión Pulmonar de Monóxido de Carbono (DLCO).
- Volúmenes pulmonares.
- Test de caminata de 6 minutos (TM6): distancia recorrida, Índice de Borg.37,39
- Saturación de oxígeno aire ambiente (SaO2 AA) basal.
- Gases arteriales basales.
- Características imagenológicas: tipo y extensión de lesión radiográfica, tipo de lesión tomográfica.
Grado de severidad de lesiones
1. Apariencia normal y/o trivial: es decir, lesiones mínimas que el evaluador considera como inactivas.
2. Leve: lesiones que ocupan menos del 25% de la cavidad torácica y sin cavitación visible.
3. Moderada: las lesiones de grado mayor, cuya totalidad, incluso si bilateral, no excede un área equivalente a la totalidad de un pulmón. Incluye cavidades menores a 2 cm de diámetro.
4. Severa: lesiones que implican una superficie mayor a la totalidad de un pulmón, incluye cavidades mayores a 2 cm de diámetro.
- Exacerbaciones
- Evidencia de infección respiratoria agregada:
- Reporte de microorganismos (bacterias, virus, hongos, parásitos).
- Técnica diagnóstica (cultivo, técnicas moleculares como Reacción en Cadena de la Polimerasa (PCR), serológicos, hisopado nasofaríngeo).
- Inmunizaciones (Anexo 3)4,34
- Calidad de vida. 31,35-39 Score de Cuestionario de enfermedad respiratoria crónica (CRQ-SAS)
- Rehabilitación respiratoria: la Rehabilitación Respiratoria (RR) es definida como una intervención interdisciplinaria realizada con protocolos estandarizados en pacientes con enfermedades respiratorias crónicas, que tienen como consecuencia de su enfermedad una disminución de las actividades de la vida diaria. Los beneficiarios de la RR tienen características individuales, grupo etario, condición clínica y características funcionales que hacen necesarias diferentes modalidades de intervención.40-43
La RR puede y debe realizarse en niñas, niños y adolescentes, tomando como edad de inicio a la misma que la utilizada para la realización de exámenes funcionales y test de caminata, dependiendo de la comprensión y predisposición del niño.
Se están evaluando los efectos de la RR pulmonar en pacientes con EPPT y, según los primeros estudios realizados, mejora significativamente la capacidad de ejercicio y la calidad de vida de los pacientes. Es fundamental la valoración funcional y de calidad de vida del paciente al inicio y al término de la RR. En pacientes estables, se recomienda la reevaluación a los 3 y 6 meses, y queda a criterio del médico tratante adicionar otras evaluaciones. 27-30,39
m) Ecocardiograma Doppler color:
Evaluar Hipertensión pulmonar (HTP) por enfermedad post tuberculosis.44,45
e) Cronograma de trabajo
Una vez la historia clínica se encuentre disponible para su uso en REDCap, permanecerá abierta para uso de los diferentes coordinadores de cada región. Por lo tanto, la fecha de inicio puede ser diferente en cada una de las mismas. Los pacientes serán evaluados al ingreso al registro, a los 6 y a los 12 meses.
La intención del grupo de trabajo a corto plazo es realizar un primer análisis a los 6 y 12 meses, respectivamente.
En una etapa posterior, la intención es mantener la base de datos de pacientes activa para futuras evaluaciones.
Análisis estadístico
Análisis de las variables:
Se aplicarán métodos de estadística descriptiva para caracterizar la muestra según el tipo de variables y se realizarán los cruces necesarios entre ellas.
Se presentará un resumen numérico mediante tablas que incluirán frecuencias absolutas y relativas porcentuales. Además, se calcularán medidas de tendencia central (media y mediana), medidas de posición (cuartiles, percentiles, entre otras) y medidas de dispersión (rango intercuartílico, rango, desviación estándar y coeficiente de variación). Análisis multivariado, significación estadística y correlación, para comparación de los grupos según sus características sociodemográficas, clínicas y funcionales.
Para el resumen gráfico, se emplearán boxplots, histogramas y gráficos de dispersión, seleccionados según los requerimientos del análisis.
Consideraciones éticas
Se solicitará el aval institucional de ALAT para la ejecución del proyecto. Además, el estudio podrá ser evaluado por los comités de ética, investigación y/o docencia de las instituciones a las que pertenezcan los participantes que registren variables en la plataforma REDCap, si así lo requieren las normas institucionales.
Cabe destacar que este estudio no implica ninguna intervención de riesgo para los pacientes ni modificaciones en su atención o tratamiento. Únicamente utilizará la información generada a partir de los estudios realizados en el manejo de su EPPT.
Los estudios epidemiológicos que requieren el análisis de documentos como fichas clínicas y resultados de estudios pueden realizarse sin el consentimiento expreso de los pacientes, siempre que se garantice la confidencialidad de su información.
No obstante, es fundamental que todos los centros involucrados informen a los pacientes, durante las entrevistas iniciales, sobre la posible utilización de los datos de sus fichas con fines de investigación y educación. Para ello, se podrá solicitar la firma de un consentimiento informado, autorizando el uso de dicha información. En el caso de pacientes pediátricos, el mismo deberá ser brindado por los padres o tutores legales y, si corresponde, el asentimiento informado del menor.46
El presente protocolo cumple con las disposiciones éticas establecidas por la Declaración de Helsinki (WMA, 2013),47 las Directrices del CIOMS (2016),48 la Convención de los Derechos del niño, Belmont Report,49 el Pacto de San José de 1969.50 Normas ISO 14155:2020 de Buenas Prácticas Clínicas en Investigación Médica,51 ICH-GCP, International Council for Harmonisation-Good Clinical Practice, E6(R2), 201652 y las legislaciones nacionales pertinente de los países involucrados, tales como la Resolución 8430 de 1993 (Colombia)53 y la Ley 25.326 (Argentina),54 la Norma Oficial Mexicana NOM-012-SSA3-2012,55 entre otras. Además, la Ley de Protección de Datos Personales de los diferentes países: Ley 25.326 (Argentina), Ley General de Protección de Datos (LGPD, Brasil),56 Resolución 466/12 (Brasil), la Ley 20.120 del 2006 de Chile,57 el Reglamento de Perú, 014-2011-SA58 y en Ecuador, el Reglamento de información confidencial en el Sistema Nacional de Salud (Acuerdo Ministerial 5216-A Registro Oficial Suplemento 427 del 29/01/2015).
Los investigadores y toda la red que participe en la obtención, recolección y análisis de los datos se comprometen a conservar la confidencialidad de la información obtenida. A tal fin, se firmará un acuerdo de confidencialidad de los datos.
El modelo de consentimiento informado de cada uno de los pacientes y el formulario del acuerdo de confidencialidad se incluyen en el anexo 4.
Divulgación de resultados obtenidos: proyecciones futuras y planes de implementación
Con la obtención de los resultados del proyecto, se prevé su difusión, en primera instancia, con referentes científicos y de atención de los casos de TB durante los próximos congresos científicos de ALAT y se propondrán para su publicación en la revista Respirar, a medida que se logren los avances. Se estima publicar un primer avance en el año 2026.
La recolección y divulgación de los resultados servirán para poner de manifiesto la realidad de la magnitud de la EPPT en Latinoamérica.
Conclusiones
Habiendo analizado las publicaciones existentes y propuesto las recomendaciones para el manejo de la enfermedad pulmonar post tuberculosis (EPPT) publicadas con anterioridad,8 creemos que es necesario la confección de un registro que permita la evaluación y estudio de nuestros pacientes, para reducir las discapacidades y los costos catastróficos asociados, con el propósito de conocer la carga estimada de la EPPT en Latinoamérica.
Este estudio no solo es factible, sino también necesario y oportuno. Su impacto trasciende el ámbito científico ya que tiene el potencial de mejorar la calidad de vida de miles de personas afectadas por TB en América Latina. La creación de un registro regional permitirá generar evidencia sólida para optimizar el diagnóstico, tratamiento y rehabilitación de la EPPT, asegurando un enfoque de atención integral y sostenible, que podría influir en la formulación de políticas públicas que contemplen no solo la curación de la TB activa, sino también el abordaje de sus secuelas a largo plazo. Esta experiencia regional podrá servir como modelo replicable en otras áreas de alta carga y promover un cambio de paradigma hacia una atención centrada en la persona, con enfoque preventivo, continuo y basado en evidencia a nivel global.
Financiamiento: los autores declaran que el trabajo no tuvo financiamiento.
Conflictos de interés: los autores declaran que no tienen conflictos de intereses relacionados con el tema de esta publicación.
Declaración de cumplimiento ético: el presente estudio corresponde a un registro observacional, sin intervención, basado en el uso secundario de datos clínicos anonimizados, por lo que no requirió aprobación de un comité de ética central. No obstante, se solicitó el aval institucional de la Asociación Latinoamericana de Tórax (ALAT), fue aprobado por el comité de ética del Instituto Vaccarezza y será evaluado por los comités de ética locales de los centros participantes, de acuerdo con las normativas vigentes de cada institución. El estudio se realizó conforme a la Declaración de Helsinki y las directrices del CIOMS.
Contribuciones de los autores: conceptualización y administración del proyecto: SJI, GBM. Supervisión y codirección: SSF, JLF. Metodología e investigación: FB, MRQ, MABG, DH, EHF.
Curaduría de datos y análisis formal: PFE, YSM. Control de calidad y validación: CPM, FLT. Redacción – borrador original: SJI, SSF, PFE. Redacción – revisión y edición: todos los autores.
El Editor en Jefe, Dr. Francisco Arancibia, realizó el seguimiento del proceso de revisión y aprobó este artículo.
Referencias
1. Allwood BW, van der Zalm MM, Amaral AFS, Byrne A, Datta S, Egere U et al. Post-tuberculosis lung health: perspectives from the First International Symposium. Int J Tuberc Lung Dis 2020; 24(8):820-828. https://doi.org/10.5588/ijtld.20.0067
2. Van Kampen SC, Wanner A, Edwards M, Harris AD, Kirenga BJ, Chakaya J et al. international research and guidelines on post-tuberculosis chronic lung disorders: a systematic scoping review. BMJ Glob Health 2018;3(4):e000745. https://doi.org/10.1136/bmjgh-2018-000745
3. Migliori GB, Marx FM, Ambrosino N, Zampogna E, Schaaf HS, Van Der Zalm MM et al. Clinical standards for the assessment, management and rehabilitation of post-TB lung disease. Int J Tuberc Lung Dis 2021; 25(10):797-813. https://doi.org/10.5588/ijtld.21.0425
4. Stolz D, Mkorombindo T, Schumann DM, Agusti A, Ash SY, Bafadhel M, et al. Towards the elimination of chronic obstructive pulmonary disease: a Lancet Commission. Lancet 2022;400(10356):921-972. https://doi.org/10.1016/S0140-6736(22)01273-9
5. GOLD. Global Strategy for Diagnosis, Management and Prevention of Chronic Obstructive Pulmonary Disease. 2025. [Internet]. [Consultado 3 jul 2012]. Disponible en: www.goldcopd.org
6. Meghji J, Simpson H, Squire SB, Mortimer K. A Systematic Review of the Prevalence and Pattern of Imaging Defined Post-TB Lung Disease. PLoS One 2016;11(8):e0161176. https://doi.org/10.1371/journal.pone.0161176
7. Ministerio Salud Argentina. Boletín tuberculosis 2024. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.argentina.gob.ar/sites/default/files/2024/04/boletin_tuberculosis_2024_1642024.pdf
8. Inwentarz SJ, Migliori GB, Lagrutta L, Bornengo F, Falco JL, de Sosa-Márquez Y et al. Recomendaciones para el manejo de la enfermedad pulmonar post tuberculosis. Respirar 2024;16(3):151-159. https://doi.org/10.55720/respirar.16.3.6
9. Byrne A, Allwood B, Schoeman I, Johnston J, Kalyatanda G, Makanda G et al. "Post tuberculosis": the urgent need for inclusion of lung health outcomes in tuberculosis treatment trials. Eur Respir J 2023; 62: 2300950. https://doi.org/10.1183/13993003.00950-2023
10. Silva DR, Pontali E, Kherabi Y, Dambrosio L, Centis R, Migliori GB. Post-TB Lung Disease: Where are we to Respond to This Priority? Arch Bronconeumol 2025;61(5):262-263. https://doi.org/10.1016/j.arbres.2025.03.001
11. Tomeny EM, Nightingale R, Chinoko B, Nikolaidis GF, Madan JJ, Worral E et al. TB morbidity estimates overlook the contribution of post-TB disability: evidence from urban Malawi. BMJ Glob Health 2022;7(5):e007643. https://doi.org/10.1136/bmjgh-2021-007643
12. Nightingale R, Carlin F, Meghji J, McMullen K, Evans D, van der Zalm MM et al. post-TB health and wellbeing. Int J Tuberc Lung Dis 2023;27(4):248-283. https://doi.org/10.5588/ijtld.22.0514
13. Allwood BW, Byrne A, Meghji J, Rachow A, van der Zalm MM, Schoch OD. Post-Tuberculosis Lung Disease: Clinical Review of an Under-Recognised Global Challenge. Respiration 2021;100(8):751-763. https://doi.org/10.1159/000512531
14. Visca D, Ambrosio L, Centis R, Pontali E, Tiberi S, Migliori GB. Post-TB disease: a new topic for investigation - and why it matters. Int J Tuberc Lung Dis 2021;25(4):258-261. https://doi.org/10.5588/ijtld.21.0040
15. Dodd PJ, Yuen CM, Jayasooriya SM, van der Zalm MM, Seddon JA. Quantifying the global number of tuberculosis survivors: a modelling study. Lancet Infect Dis 2021;21(7):984-992. https://doi.org/10.1016/S1473-3099(20)30919-1
16. Pasipanodya JG, McNabb SJ, Hilsenrath P, Bae S, Lykens K, Vecino E et al. Pulmonary impairment after tuberculosis and its contribution to TB burden. BMC Public Health 2010;10:259. https://doi.org/10.1186/1471-2458-10-259
17. Amaral AF, Coton S, Kato B, Tan WC, Studnicka M, Janson C et al. Tuberculosis associates with both airflow obstruction and low lung function: BOLD results. Eur Respir J 2015; 46(4):1104-12. https://doi.org/10.1183/13993003.02325-2014
18. Allwood BW, Stolbrink M, Baines N, Louw E, Wademan DT, Lupton-Smith A et al. Persistent chronic respiratory symptoms despite TB cure is poorly correlated with lung function. Int J Tuberc Lung Dis 2021; 25(4):262-270. https://doi.org/10.5588/ijtld.20.0906
19. Menzies NA, Quaife M, Allwood BW, Byrne AL, Coussens AK, Harries AD et al. Lifetime burden of disease due to incident tuberculosis: a global reappraisal including post-tuberculosis sequelae. Lancet Glob Health 2021; 9(12):e1679-e1687. https://doi.org/10.1016/s2214-109x(21)00367-3
20. Miller TL, Wilson FA, Pang JW, Beavers S, Hoger S, Sharnprapai S et al. Mortality hazard and survival after tuberculosis treatment. Am J Public Health 2015; 105(5):930-7. https://doi.org/10.2105/AJPH.2014.302431
21. Mpagama SG, Msaji KS, Kaswaga O, Zurba L, Mbelele PM, Allwood BW et al. The burden and determinants of post-TB lung disease. Int J Tuberc Lung Dis 2021; 25(10):846-853. https://doi.org/10.5588/ijtld.21.0278
22. Chesov D, Butov D, Reimann M, Heyckendorf J, Myasoedov V, Butov T et al. Impact of lung function on treatment outcome in patients with TB. Int J Tuberc Lung Dis 2021; 25(4):277-284. https://doi.org/10.5588/ijtld.20.0949
23. Kayongo A, Nyiro B, Siddharthan T, Kirenga B, Checkley W, Joloba ML et al. Mechanisms of lung damage in tuberculosis: implications for chronic obstructive pulmonary disease. Front Cell Infect Microbiol 2023; 13:1146571. https://doi.org/10.3389/fcimb.2023.1146571
24. Harris PA. Research electronic data capture (REDCAP) – A metadata-driven methodology and workflow process for providing translational research informatics support. J Biomed Inform 2009;42(2):377-381. https://doi.org/10.1016/j.jbi.2008.08.010
25. Tiberi S, Muñoz-Torrico MM, Rahman A, Krutikov M, Visca D, Rossato-Silva D et al. Managing severe tuberculosis and its sequelae: from intensive care to surgery and rehabilitation. J Bras Pneumol 2019;45(2):e20180324. https://doi.org/10.1590/1806-3713/e20180324
26. Muñoz-Torrico M, Cid-Juárez S, Gochicoa-Rangel L, Torres Bouscolet L, Salazar-Lezama MA, Villareal-Velarde H et al. Functional impact of sequelae in drug-susceptible and multidrug-resistant tuberculosis. Int J Tuberc Lung Dis 2020;24(7):700-705. https://doi.org/10.5588/ijtld.19.0809
27. Sivaranjini S, Vanamail P, Eason J. Six-minute Walk test in people with tuberculosis sequelae. Cardiopulm Phys Ther J 2010;21(3):5-10.
28. Anidi IU, Kirenga B, Fennelly KP. Rehabilitación pulmonar para la enfermedad pulmonar post tuberculosa. Am J Respir Crit Care Med 2023;208(11):1246-1247. https://doi.org/10.1164/rccm.202309-1571LE
29. Fernandez LC, Cairme GB. The Benefits of Pulmonary Rehabilitation Program on Post-Tuberculosis Bronchiectasis. Internat J Clin Med 2022;13:561-570. https://doi.org/10.4236/ijcm.2022.1312042
30. Zenteno AD, Torres PG, Cox LV. Indicaciones de rehabilitación respiratoria en niños y adolescentes con enfermedades respiratorias crónicas. Rev Chil Enferm Respir 2022;38(1):26-32. https://doi.org/10.4067/S0717-73482022000100026
31. Kim DY, Mo YH, Kim KW, Hong SM, Park A, Jang BH et al. Feasibility of Home-Based Pulmonary Rehabilitation of Pediatric Patients with Chronic Respiratory Diseases. Children 2024;11(5):534. https://doi.org/10.3390/children11050534
32. Nkereuwem E, Agbla S, Sallahdeen A, Owolabi O, Sillah AK, Genekah M et al. Reduced lung function and health-related quality of life after treatment for pulmonary tuberculosis in Gambian children: a cross-sectional comparative study. Thorax 2023; 78(3): 281-287. https://doi.org/10.1136/thorax-2022-219085
33. Martinez L, Gray DM, Botha M, Nel M, Chaya S, Jacobs C et al. The Long-Term Impact of Early-Life Tuberculosis Disease on Child Health: A Prospective Birth Cohort Study. Am J Respir Crit Care Med 2023;207(8):1080-1088. https://doi.org/10.1164/rccm.202208-1543oc
34. Nkereuwem O, Nkereuwem E, Owolabi O, John P, Egere U, Mortimer K et al. Perspectives of TB survivors and policymakers on post-TB disability. Public Health Action 2023;13(1):17-22. https://doi.org/10.5588/pha.22.0050
35. Nasiri MJ, Silva DR, Fommasi F, Zahmatkesh MM, Tajabadi Z, Khelghati F et al. Vaccination in post-tuberculosis lung disease management: a review of the evidence. Pulmonology 2025;31(1):2416801. https://doi.org/10.1016/j.pulmoe.2023.07.002
36. Datta S, Gilman RH, Montoya R, Quevedo Cruz L, Valencia T, Huff D et al. Quality of life, tuberculosis and treatment outcome: a case-control and nested cohort study. Eur Respir J 2020;56(2):1900495. https://doi.org/10.1183/13993003.00495-2019
37. Llanos-Tejada F, Ponce-Chang C. Depresión y adherencia en personas afectadas con tuberculosis. Una exploración preliminar de datos. Rev Neuropsiquiatr 2019;82(2):104-109. https://doi.org/10.20453/rnp.v82i2.3536
38. Valero-Moreno S, Castillo-Corullón S, Vicente J, Prado-Gascó VJ, Pérez-Marín M, Montoya-Castilla I et al. Cuestionario de enfermedad respiratoria crónica (CRQ-SAS): análisis de las propiedades psicométricas. Arch Argent Pediatr 2019;117(3). https://doi.org/10.5546/aap.2019.149
39. Vigil L, Güell MR, Morante F, López de Santamaría E, Sperati F, Guyatt G et al. Validez y sensibilidad al cambio de la versión española autoadministrada del cuestionario de la enfermedad respiratoria crónica (CRQ-SAS). Arch Bronconeumol 2011;47(7):343–349. https://www.archbronconeumol.org/es-validez-sensibilidad-al-cambio-version-articulo-S0300289611000937
40. Silva DR, Queiroz-Mello FC, Galvão TS, Dalcolmo M, dos Santos APC et al. Pulmonary Rehabilitation in Patients With Post-Tuberculosis Lung Disease: A Prospective Multicentre Study. Arch Bronconeumol 2025;61(10):603-609. https://doi.org/10.1016/j.arbres.2025.02.007
41. Pontali E, Silva DR, Marx FM, Caminero JA, Centis R, Dambrosio L et al. Breathing Back Better. A State of the Art on the Benefits of Functional Evaluation and Rehabilitation of Post-Tuberculosis and Post-COVID Lungs. Arch Bronconeumol 2022; 58(11):754-763. https://doi.org/10.1016/j.arbres.2022.05.010
42. Migliori GB, Caminero Luna J, Kurhasani X, van den Boom M, Visca D, Dambrosio L et al. History of prevention, diagnosis, treatment and rehabilitation of pulmonary sequelae of tuberculosis. Presse Med 2022; 51(3):104112. https://doi.org/10.1016/j.lpm.2022.104112
43. Silva DR, Freitas AA, Guimarães AR, Dambrosio L, Centis R, Muñoz-Torrico M et al. Post-tuberculosis lung disease: a comparison of Brazilian, Italian, and Mexican cohorts. J Bras Pneumol 2022; 48(2):e20210515. https://doi.org/10.36416/1806-3756/e20210515
44. Walsh KF, Lui JK. Post-tuberculosis pulmonary hypertension: a case of global disparity in health care. Lancet Glob Health 2022;10(4):e476. https://doi.org/10.1016/S2214-109X(22)00042-0
45. Chen Y, Liu C, Lu W, Li M, Hadadi C, Wang EW et al. Clinical characteristics and risk factors of pulmonary hypertension associated with chronic respiratory diseases: a retrospective study. J Thorac Dis 2016;8:350–8. https://doi.org/10.21037/jtd.2016.02.58
46. Asamblea General de las Naciones Unidas. Convención sobre los Derechos del Niño. 1989. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.unicef.org
47. Declaración de Helsinki: Principios éticos para las investigaciones médicas en seres humanos. 2013. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.wma.net/policies-post/wma-declaration-of-helsinki-ethical-principles-for-medical-research-involving-human-subjects/
48. Consejo de Organizaciones Internacionales de las Ciencias Médicas (CIOMS). Directrices éticas internacionales para la investigación relacionada con la salud que involucra seres humanos. 2016. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://cioms.ch/publications/product/international-ethical-guidelines-for-health-related-research-involving-humans/
49. The National Commission for the Protection of Human Subjects of Biomedical and Behavioral Research. The Belmont Report: Ethical Principles and Guidelines for the Protection of Human Subjects of Research. Washington, D.C.: U.S. Department of Health, Education, and Welfare; 1979. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.hhs.gov/ohrp/regulations-and-policy/belmont-report/index.html
50. Convención Americana sobre Derechos Humanos (Pacto de San José): Organización de los Estados Americanos (OEA). Convención Americana sobre Derechos Humanos (Pacto de San José). San José: OEA; 1969. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.oas.org
51. ISO 14155:2020: International Organization for Standardization. ISO 14155:2020: Clinical investigation of medical devices for human subjects – Good clinical practice. Geneva: ISO; 2020. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.iso.org
52. ICH-GCP International Council for Harmonisation of Technical Requirements for Pharmaceuticals for Human Use (ICH). E6(R2): Guideline for Good Clinical Practice. Geneva: ICH; 2016. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.ich.org
53. Ministerio de Salud de Colombia. Resolución 8430 de 1993: Normas científicas, técnicas y administrativas para la investigación en salud. 1993. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.minsalud.gov.co
54. Congreso de la Nación Argentina. Ley 25.326 de Protección de los Datos Personales. 2000. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.argentina.gob.ar
55. Congreso General de los Estados Unidos Mexicanos. Ley Federal de Protección de Datos Personales en Posesión de los Particulares. Ciudad de México: Diario Oficial de la Federación; 2010. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.dof.gob.mx/
56. Presidência da República do Brasil. Lei Geral de Proteção de Dados Pessoais (Lei n.º 13.709, de 14 de agosto de 2018). Brasília: Diário Oficial da União; 2018. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.planalto.gov.br/
57. República de Chile. Ley N.º 20.120: Sobre la investigación científica en el ser humano, su genoma, y prohíbe la clonación humana. Santiago de Chile: Biblioteca del Congreso Nacional de Chile; 2006. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.bcn.cl
58. República del Perú. Decreto Supremo N.º 014-2011-SA: Reglamento de Ensayos Clínicos. Lima: Ministerio de Salud; 2011. [Internet]. [Consultado 3 jun 2025]. Disponible en: https://www.gob.pe
Anexos
Anexo 1. Historia clínica
Fecha de captación de paciente: dd/mm/aaaa
Número Identificatorio (automático): ___________
Centro: ______________________________
DATOS PERSONALES/DEMOGRÁFICOS
- Nombre
- Apellido
- Ciudad:
- País de Residencia:
- País de origen/nacionalidad:
- Fecha de nacimiento: dd/mm/aaaa
- Edad_____años
- Género al nacimiento
⸰ Femenino
⸰ Masculino
- Nivel educativo:
⸰ Primario Completo Incompleto
⸰ Secundario Completo Incompleto
⸰ Terciario (técnico) Completo Incompleto
⸰ Universitario Completo Incompleto
- Cobertura médica
⸰ Sí
seguridad social
seguro público
seguro privado
⸰ No
- Peso: kg
- Altura: cm
ANTECEDENTES DE ENFERMEDAD TUBERCULOSA:
- Tuberculosis previa
⸰ AÑO (en caso de episodios múltiples, indicar el último):
⸰ Número de episodios previos confirmados (si corresponde)
- Presentación TB
⸰ Pulmonar
⸰ Extrapulmonar
⸰ Diseminada
- Tiempo de inicio de síntomas por TB hasta inicio de tratamiento en meses:
- Fecha/año de finalización de tratamiento antituberculosis: dd/mm/aaaa (permitir UNK/UNK/aaaa)
- Diagnóstico de la TB (último episodio)
⸰ Empírico clínico/radiológico:
Si
No
⸰ Bacteriológico: muestra que sustentó el diagnóstico:
• Si
Esputo
Esputo inducido
Lavado Bronquiolo Alveolar
Aspirado gástrico
Heces
Otros/especifique
• No
⸰ Baciloscopia
⸰ Cultivo
Lowenstein Jenssen
MGIT
LPA
⸰ Pruebas moleculares
GenXpert
GeneXpert Ultra
GeneXpert XDR
Truenat
BD-Max
TB-LAM
Abbott Real Time MTB
Fluorotype MTB-DR
Roche MTB Rif/INH
⸰ Secuenciación genómica
Si
No
⸰ Anatomía patológica
Si
Sitio anatómico/órgano/tejido
Descripción (casillero texto libre)
No
- Sensibilidad al inicio del tratamiento:
⸰ Si
⸰ No
En caso de resistencia: precisar resistencia a qué droga (H, R, E, Z, FQ, ISL, etc.) (pestaña aparte)
- Tratamiento recibido:
⸰ Drogas de primera línea
⸰ Drogas de segunda línea
- Duración tratamiento: meses
- Tratamiento
⸰ Supervisado
Si
DOT
VOT
⸰ Autoadministrado
Si
Regular: mayor o igual al 80% de las tomas en el tiempo indicado.
Irregular: menor al 80% de las tomas en el tiempo indicado.
- Pérdidas de seguimiento
⸰ Si
⸰ No
- Reacción adversa medicamentosa
⸰ Si
Tipo (casillero)
Cutánea
Hepática
Renal
Hematológica
DRESS
Otras (+casillero)
Severa (requieren internación)
⸰ No
Requirió cambio de medicación
Si
No
ANTECEDENTES PATOLÓGICOS/COMORBILIDADES
- Diabetes
⸰ Si
Tiempo de evolución
Controlada
No controlada
⸰ No
- Hiperreactividad bronquial/broncoespasmo
⸰ Si
⸰ No
- VIH
⸰ Si
Tiempo de evolución
TARV
SI
NO
⸰ No
- Inmunodeficiencias no VIH
⸰ Si
⸰ No
- Enf. Hemato- oncológicas:
⸰ Si - Especificar enfermedad (casillero texto libre)
Uso de inmunosupresores
Si - Especificar (casillero texto libre)
No
⸰ Otras enfermedades inmunosupresoras: especificar
EXPOSICIÓN LABORAL/MEDIOAMBIENTAL
- Vivienda
⸰ Urbana
⸰ Rural
⸰ Situación de calle
- Exposición: Laboral/Pasatiempos (de riesgo de enfermedad respiratoria)
- Si
⸰ Minerías
⸰ Siderometalúrgica
⸰ Fábrica de papel
⸰ Fundiciones
⸰ Madereras
⸰ Recolección de algodón
⸰ Panaderos
⸰ Soldadores
⸰ Pintores
⸰ Escultores
⸰ Otros
- No
- Hábitos tóxicos:
⸰ Si
Tabaquismo:
Ex fumador
fumador actual
Paquetes/año
Consumo de drogas:
Inhalados
Inyectables
Alcohol:
Otras
⸰ No
EVALUACIÓN EPPT
Estos datos deben ser recabados al ingreso al registro y reevaluados a los 6 y 12 meses
- Síntomas respiratorios crónicos o persistentes:
⸰ Tos
Seca
Productiva
Mixta
Diurna
Nocturna
⸰ Expectoración
⸰ Dolor u opresión torácica
⸰ Dolor
⸰ Hemoptisis
⸰ Despertares nocturnos
⸰ Fiebre
⸰ Sibilancias
Diurnas
Nocturnas
⸰ Disnea - Escala mMRC
Grado 0: Ausencia de disnea al realizar ejercicio intenso.
Grado 1: Disnea al andar deprisa en llano o al subir una pendiente.
Grado 2: La disnea le produce una incapacidad de mantener el paso de otras personas de la misma edad caminando en llano o tener que parar para descansar al andar en llano a su propio paso.
Grado 3: La disnea hace que tenga que parar a descansar al andar unos 100 metros o pocos minutos después de andar en llano.
Grado 4: La disnea impide al paciente salir de casa o aparece con actividades como vestirse o desvestirse.
- Tratamiento controlador
⸰ Uso de LAMA
Si
Tiempo de uso (meses)
No
⸰ Uso de LABA
Si
Tiempo de uso (meses)
No
⸰ Uso de corticoides
Si
Tiempo de uso (meses)
No
⸰ Otros fármacos si no
- Exacerbaciones respiratorias
Evento caracterizado por disnea y/o tos y esputo que empeora en relación con su estado basal en un periodo menor a 14 días, que puede ir acompañado de taquipnea y/o taquicardia, y a menudo se asocia con un aumento de la inflamación local y sistémica causada por una infección de las vías respiratorias, contaminación u otra agresión a las vías aéreas. (64)
⸰ Si - Número/año
⸰ No
- Sobreinfección respiratoria:
⸰ Si (especificar método y microorganismo)
Hisopado nasofaríngeo
Esputo
BAL
PCR virus respiratorios
Antígenos
Serologías
Microorganismo (casillero texto libre)
⸰ No
- Uso de antimicrobianos
⸰ Si
Tiempo (en días)
Betalactámicos
Cefalosporinas
Macrólidos
Fluoroquinolonas
Otros fármacos
⸰ No
- Colonización crónica
⸰ Si
Microorganismo
Tratamientos supresores
Si
Nebulizados
Orales
No
⸰ No
- Ingresos hospitalarios por exacerbaciones respiratorios/año
- Si (casillero texto libre para número de ingresos)
- No
VALORACIÓN INICIAL
- Saturometría
⸰ Casillero texto libre para número - AA
- Pruebas de Función Pulmonar
⸰ Espirometría:
FVC (L), (%)
Pre
Post
FEV1 (L) (%)
Pre
Post
FEV1/FVC (%)
Pre
Post
FEF 25/75% (L/seg) (%)
Pre
Post
⸰ Volúmenes pulmonares por pletismografía o por dilución
TLC (L)
TGV (L)
RV (L)
RV/TLC (%)
⸰ Difusión pulmonar de monóxido de carbono (DLCO)
DLCO unc
DLCO cor
VA
Kco
⸰ Patrón obstructivo
Si
Leve 70-100%
Moderado 50-69%
Severo <50%
No
⸰ Patrón no obstructivo
Si
- 70 - 65% Leve ()
- 64 - 50% Moderado ()
- 49- 35% Grave ()
- < 34% Muy Grave ()
- No
- Test de marcha 6 minutos
⸰ Distancia o metros recorridos en 6 minutos —-------
⸰ Valor teórico —-----
⸰ % teórico —-----
⸰ LIN—---
⸰ Disnea
SI ( )
NO ()
BORG (casillero para puntuación).
⸰ Presenta desaturación al final del ™
SI
NO
- Evaluación radiológica
⸰ Apariencia normal
Si
No
⸰ Cavitación
Si
Única
Múltiple
Diámetro mayor <2 cm
Diámetro mayor entre 2 y 4 cm
Diámetro mayor >4 cm
No
- Clasificación radiológica de lesiones pulmonares según su extensión (descripción en el texto):
⸰ ≤ al 25% de la cavidad torácica
⸰ del 25% al 49% de la cavidad torácica
⸰ ≥ al 50% de la cavidad torácica
- Evaluación de la Tomografía de Tórax de Alta resolución y cortes finos (se puede seleccionar más de 1):
⸰ Bronquiectasias
⸰ Bullas
⸰ Neumotórax
⸰ Engrosamiento pleura
⸰ Tractos fibrosos
⸰ Fibrosis
⸰ Abscesos
⸰ Cavitaciones o cavidades detergidas
⸰ Nódulos
⸰ Atelectasias
⸰ Consolidaciones
⸰ Intersticiopatías
- Imagen radiográfica (alta tratamiento TB)
- Imagen tomográfica (según disponibilidad)
- Ecocardiograma Doppler (según disponibilidad)
⸰ Hipertensión pulmonar
SI
NO
Valor PSAP: ___ mmHg
- Cuestionario de Enfermedad Respiratoria Crónica (CRQ-SAS)
⸰ Disnea
⸰ Fatiga
⸰ Función emocional
⸰ Control de la enfermedad.
⸰ Score total
- Rehabilitación respiratoria
⸰ Indicación
Si
No
⸰ Inicio
Si
No
- Inmunizaciones (se puede más de una opción)
⸰ Influenza
⸰ Neumococo
⸰ Covid-19
⸰ Pertussis
⸰ Herpes Zoster
⸰ Difteria
⸰ Tétanos
⸰ Sarampión, paperas y rubéola
⸰ Virus sincitial respiratorio
Anexo 2.
Cuestionario de Enfermedad Respiratoria Crónica (CRQ-SAS)
Instrucciones: Este cuestionario está diseñado para comprender cómo su enfermedad respiratoria afecta su vida diaria. Por favor, responda a cada pregunta de la manera más precisa posible, basándose en su experiencia durante las últimas dos semanas.
1. Disnea (dificultad para respirar)
Indique en qué medida ha experimentado dificultad para respirar durante las siguientes actividades en las últimas dos semanas:
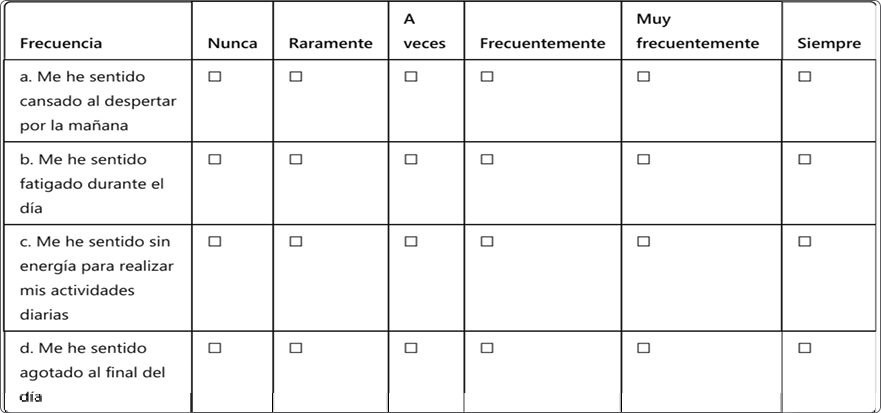
2. Fatiga
Indique con qué frecuencia ha sentido fatiga o cansancio en las últimas dos semanas
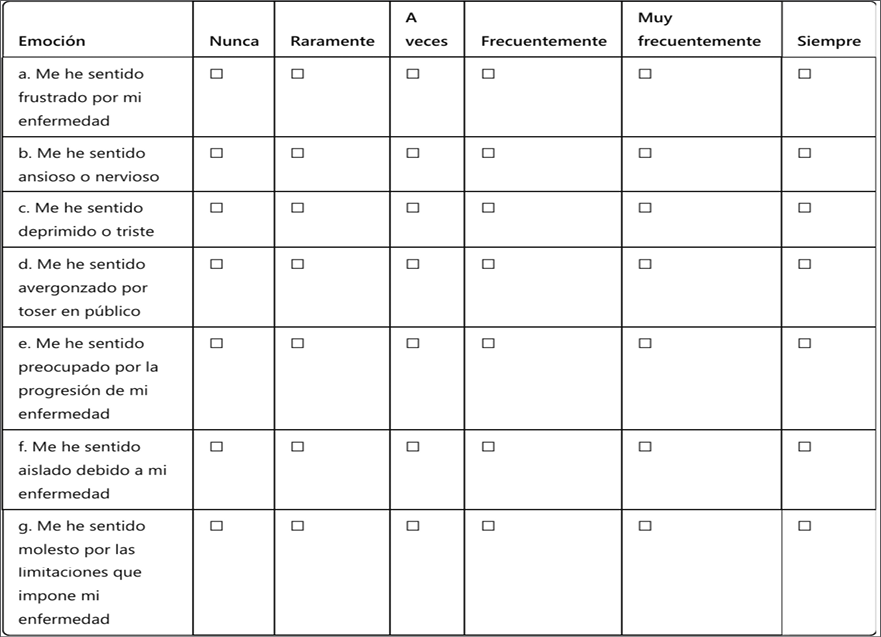
3. Función Emocional
Indique con qué frecuencia ha experimentado las siguientes emociones en las últimas dos semanas debido a su enfermedad respiratoria:
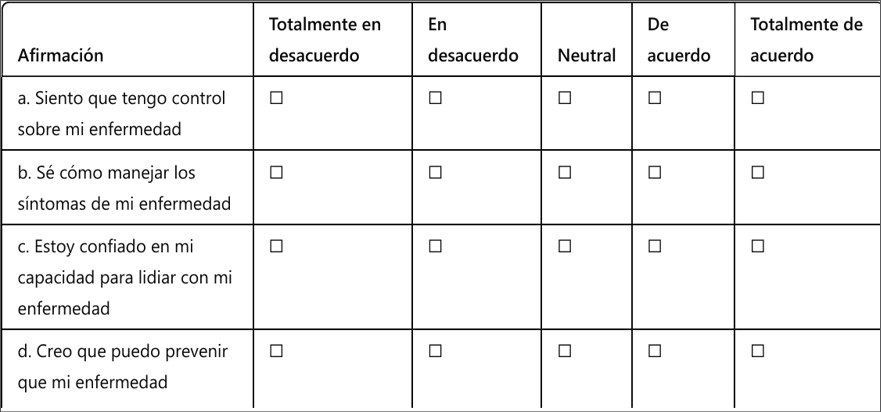
4. Control de la Enfermedad:
Indique en qué medida está de acuerdo con las siguientes afirmaciones sobre su capacidad para manejar su enfermedad respiratoria en las últimas dos semanas:
Comentarios Adicionales:
Si tiene algún comentario o desea proporcionar información adicional sobre cómo su enfermedad respiratoria afecta su vida diaria, por favor utilice el espacio a continuación:
----------------------------------------------------------------------------------
----------------------------------------------------------------------------------
Instrucciones para la puntuación:
Disnea: cada ítem se puntúa de 1 (ninguna) a 7 (muy severa).
Fatiga y función emocional: cada ítem se puntúa de 1 (nunca) a 7 (siempre). Control de la enfermedad: cada ítem se puntúa de 1 (totalmente en desacuerdo) a 5 (totalmente de acuerdo).
Las puntuaciones más altas indican una mejor calidad de vida relacionada con la salud en cada dimensión evaluada.
Anexo 3.
Vacunación recibida
Recomendaciones ALAT para la vacunación de los pacientes con enfermedades pulmonares crónicas.8
|
Vacunas aplicadas |
Vacunas recomendadas |
Esquema recomendado |
|
Influenza |
anual |
|
|
Neumococo |
PCV20 o PCV 13 |
|
|
Covid-19 |
2 dosis iniciales = refuerzos semestrales |
|
|
Pertussis |
refuerzos cada 10 años |
|
|
Herpes Zoster |
2 dosis iniciales en > 50 a |
|
|
Difteria |
refuerzos cada 10 a |
|
|
tétanos |
refuerzos cada 10 a |
|
|
Sarampión, paperas y rubéola |
según epidemiología regional |
|
|
Virus sincitial respiratorio |
Mayores de 60/65 años según país. |
Anexo 4.
Modelo de consentimiento informado
CONSENTIMIENTO INFORMADO
A RECABAR POR EL MÉDICO TRATANTE
En esta institución realizamos tareas asistenciales y docentes. Es por este motivo que las historias clínicas junto con los estudios realizados son utilizadas muchas veces como base de datos para la realización de estudios de investigación y como casos clínicos de la vida real para las prácticas de nuestros alumnos y discusión en ateneos clínicos para discutir el caso entre nuestro plantel profesional y tomar una conducta médica adecuada.
Solicitamos por este medio, su autorización en forma voluntaria, para utilizar la información que allí se encuentre, manteniendo siempre el anonimato y regidos por la Ley de Protección de Datos Personales, propias de cada país.
Todos sus datos se mantendrán confidenciales y se tomarán todas las precauciones para proteger la privacidad de cada uno de nuestros pacientes. Su negativa no modificará ni alterará su diagnóstico ni su tratamiento.
Este documento quedará adjuntado a la Historia Clínica, bajo el resguardo institucional.
Las investigaciones que resulten del uso de ésta serán evaluadas por el Comité de Ética en Investigación del Instituto.
Consentimiento informado:
Habiendo leído y comprendido el texto precedente, doy mi autorización para la utilización de los datos que sean de interés de acuerdo con los términos que se describen anteriormente.
a. ͏ Doy mi autorización para el uso de mis datos para investigación
b. ͏ No doy mi autorización para el uso de mis datos para investigación
Lugar y fecha:
Nombre y apellido: DNI Firma:
Teléfono de contacto
Datos del médico tratante:
Aclaración del Nombre y Apellido Firma del médico Matrícula
Lugar y Fecha