
Artículo Original | Respirar, 2026; 18 (1): 47-58 | ISSN 2953-3414 | https://doi.org/10.55720/respirar.18.1.3
Definición de asma leve en Argentina: consenso de expertos por método Delphi
Definition of Mild Asthma in Argentina: Expert Consensus by Delphi Method
1 Hospital Dr. J.C. Perrando, Resistencia, Chaco, Argentina.
2 Hospital Central de Mendoza, Mendoza, Argentina.
3 Universidad Nacional de Cuyo, Facultad de Ciencias Médicas, Mendoza, Argentina.
4 Ministerio de Salud, Provincia de La Rioja, Argentina.
5 Hospital Nacional Baldomero Sommer, Gral. Rodríguez, Provincia de Buenos Aires, Argentina.
6 Universidad de Buenos Aires, Argentina.
7 Hospital Escuela General José de San Martín, Corrientes, Corrientes, Argentina.
Autor corresponsal:
Carlés Daniel Luis. E-mail: selracdaniel@yahoo.com.ar
Recibido:
29 julio 2025
Aprobado:
12 septiembre 2025
Resumen
Introducción: El asma leve afecta al 50–75% de los pacientes que padecen esta patología. Puede presentar exacerbaciones graves. La literatura ofrece múltiples definiciones, con discrepancias en los parámetros de control y en el tratamiento requerido para alcanzarlo. El objetivo de este trabajo fue definir el asma leve en adultos mediante consenso de expertos, para su aplicación práctica en distintos niveles de atención.
Métodos: Se realizó una revisión bibliográfica y luego se aplicó el método Delphi modificado, con tres rondas de consulta y una reunión plenaria. Participaron 19 expertos pertenecientes a las distintas regiones geográficas del país.
Resultados: Se consensuó que el asma leve se caracteriza por el control alcanzado con dosis bajas de corticoides inhalados (CI), CI/salbutamol o CI/formoterol, según necesidad. Este control se define por síntomas diurnos ≤2 veces por semana; nocturnos ≤1 vez por mes; sin limitaciones funcionales ni exacerbaciones en el último año y tener una espirometría normal. Se excluyeron los pacientes con antecedentes de asma casi fatal, internaciones, tabaquismo activo, comorbilidades relevantes o embarazo. Se desaconsejó la monoterapia con SABA.
Conclusión: Se propone una definición operativa y retrospectiva de asma leve, basada en la intensidad del tratamiento necesario para lograr control sintomático y minimizar riesgos. Los criterios son simples y aplicables en cualquier nivel de atención.
Palabras clave: asma leve; definición; método Delphi.
Abstract
Introduction: Mild asthma affects 50–75% of patients with asthma and can progress to severe exacerbations. The literature offers multiple definitions, with discrepancies based in the definition of its control and treatment required to achieve it. The objective of our work was to create a practical definition of mild asthma in adults through expert consensus, in order to apply it at different levels of care.
Methods: A literature review was conducted, followed by the modified Delphi method, which included three rounds of consultations and a plenary meeting. Nineteen experts from various geographic regions of the country participated.
Results: By consensus, mild asthma was characterized by symptomatic control achieved with low doses of inhaled corticosteroids (ICS), ICS/salbutamol, or ICS/formoterol as needed. This control is defined as daytime symptoms occurring ≤2 times per week, nighttime symptoms occurring ≤1 time per month, no functional limitations or exacerbations in the past year, and normal spirometry. Patients with a history of near-fatal asthma, hospitalizations, active smoking, significant comorbidities, or pregnancy were excluded. SABA monotherapy was discouraged.
Conclusion: A retrospective, operational definition of mild asthma is proposed, based on the treatment intensity required to control symptoms and minimize risks. The criteria are simple and applicable to any level of care.
Keywords: mild asthma; definition; Delphi method.
Introducción
El asma es una enfermedad inflamatoria crónica de las vías respiratorias. Es una condición heterogénea, donde tanto los síntomas (disnea, sibilancias, tos, otros) así como el flujo aéreo espiratorio se caracterizan por su variabilidad en el tiempo.1,2 Afecta aproximadamente a 339 millones de personas en el mundo.3,4
En Argentina en 2018, se registraron 19.244 egresos hospitalarios y en 2020, 344 muertes por asma.5 La primera encuesta nacional de prevalencia en adultos realizada en nuestro país entre 2014 y 2015, dio cuenta de que 6 de cada 100 personas tuvieron alguna crisis en los últimos 12 meses o empleaban, al momento de ser consultados, medicación para el asma; 9 de cada 100 había tenido alguna vez asma confirmada por un médico.6
La gravedad de la enfermedad se define fundamentalmente con base en la intensidad del tratamiento necesario para controlar los síntomas y reducir el riesgo futuro. Sin embargo, en el ámbito de la atención primaria se suele asociar con la frecuencia e intensidad de los síntomas y las exacerbaciones, independientemente de la terapéutica de mantenimiento.1 Se estima que la mayoría de los pacientes, 50 a 75%, presentan enfermedad leve y solo es grave entre el 3,6 y 8%.7,8A pesar de esta alta prevalencia, el asma leve no ha sido objeto de tantas publicaciones como el asma grave.9 Estas formas están frecuentemente subdiagnosticadas y los pacientes no tienen buen control de la enfermedad.10 El término “leve” puede aplicarse a pacientes con riesgo de presentar exacerbaciones; un estudio señala que entre el 30 y el 53% de consultas a emergencias por asma corresponden a sujetos categorizados como tales.7La frecuencia de exacerbaciones graves oscila entre 0,12 y 0,77 por paciente-año en personas clasificadas como leves.11,12 En un análisis retrospectivo, el 9% de los fallecidos por asma en el Reino Unido habían sido catalogados previamente como leves.13
En las guías y recomendaciones disponibles existen diferentes definiciones de las formas leves, casi todas basadas en el tratamiento necesario para alcanzar el control (Tabla 1).1,2,14-17 Se realizó el presente trabajo con el objetivo de elaborar una definición consensuada de asma leve.
Tabla 1.
Definiciones de asma leve en mayores de 12 años según diferentes guías.
|
GUÍA |
DEFINICIÓN |
|---|---|
|
NAEPP (2020) |
Es aquella cuyo control se alcanza con: dosis bajas diarias de CI, más SABA según necesidad; o bien dosis bajas de CI y SABA según necesidad usados concomitantemente (uno después del otro). |
|
Canadian Thoracic Society (2021) |
Aquella que es bien controlada con dosis bajas de CI (o antileucotrienos) y SABA según necesidad, o bien CI/LABA según necesidad. Admiten categoría de “muy leve” que solo requiere SABA a demanda. |
|
Ministerio Salud Argentina (2023) |
Aquella que se mantiene bien controlada con escalón 2 del tratamiento de GINA 2021 (dosis bajas de CI-formoterol según necesidad). Para evaluar el control del asma debe considerarse tanto la presencia de síntomas como el riesgo futuro de exacerbaciones. |
|
Japanese guidelines (2023) |
Leve persistente: síntomas diurnos 1 o más veces por semana, pero no todos los días. Perturba vida diaria o sueño al menos 1 vez por mes, síntomas nocturnos 2 o más por mes. FEV1 ≥80%, variación PEF 20-30%. Tratamiento preferido: CI (dosis bajas a medias). |
|
NICE (2024) |
Define el asma leve indirectamente al describir el tratamiento inicial para personas con asma recién diagnosticada. En mayores de 12 años, inhalador combinado de CI/formoterol en dosis baja, según necesidad como terapia AIR. |
|
GEMA 5.5 (2025) |
La que tiene necesidades mínimas de tratamiento para mantener el control. Intermitente: escalón 1 (CI/LABA, o CI/SABA a demanda); persistente, escalón 2 (CI a dosis bajas diariamente o bien CI/LABA o SABA a demanda) |
|
GINA (2025) |
Es la que puede ser bien controlada con CI-formoterol según necesidad o con bajas dosis de CI diario (Escalones 1 y 2), |
CI: corticoides inhalados. SABA: short acting beta agonists. LABA: long acting beta agonists. AIR: Anti-inflammatory Reliever
Materiales y métodos
Un grupo de médicos neumonólogos pertenecientes a la Asociación Argentina de Medicina Respiratoria (AAMR) se reunió desde julio de 2024 con la finalidad de elaborar una definición consensuada de asma leve. Se aplicó el método Delphi modificado para realizar un consenso de expertos.
Se realizó una revisión de la literatura de los últimos 10 años (2014-2024) en Pubmed, en inglés y español, utilizando los términos “definición”, “asma leve” y “adultos”. Se incluyeron artículos primarios, guías, consensos internacionales y locales, que tuvieran al menos una definición de asma leve para pacientes adultos. Se extrajeron los criterios utilizados en estas definiciones, que fueron incluidos en el instrumento de la primera ronda.
Se aplicó el método Delphi en función de su utilidad para obtener consenso en el área de la salud en problemas en los que existen diferentes perspectivas.18 Para conformar el grupo de expertos, se invitó a participar por correo electrónico a 21 profesionales considerados expertos con base en sus publicaciones sobre el tema o en un acreditado conocimiento basado en la práctica y la experiencia; 19 aceptaron. Dieciocho de ellos tenían más de 20 años en la especialidad y uno más de 10 años. En este proceso de selección, se priorizó, además, un criterio geográfico procurando contar con representantes de todas las regiones del país.
Entre el 13 de septiembre 2024 y el 25 de noviembre 2024, se realizaron tres rondas de envío de encuestas con criterios de definición a través de formularios Google Forms. Solo la primera ronda incluyó una pregunta abierta que permitió a los expertos incluir criterios adicionales no considerados inicialmente por el grupo investigador. Los criterios enunciados se clasificaron según una escala de Likert de 7 puntos, donde 1 significaba fuertemente en desacuerdo y 7 fuertemente de acuerdo en incorporar el criterio a la definición. Se consideró que un criterio era aceptado si el 70% o más de los médicos le asignaba un puntaje de 6 o 7, y era descartado si el 70% o más respondía 1 o 2. Los criterios con puntajes intermedios fueron evaluados en las rondas siguientes.
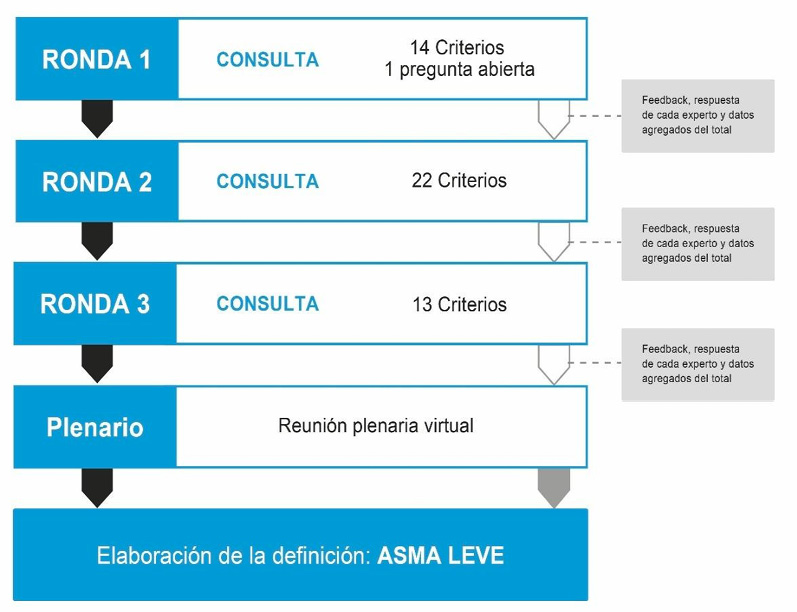
Luego de cada ronda, se envió retroalimentación con la respuesta individual del experto y la información integrada (mediana y rango intercuartil) del resto de los participantes. Se mantuvo el anonimato durante todo el proceso. El 18 de marzo de 2025, se realizó una mesa de discusión virtual por plataforma Zoom en la que participaron 16 expertos (84%). Se pusieron en consideración los criterios aprobados y, a sugerencia de los asistentes, algún otro que no había resultado ni aprobado ni rechazado en las rondas. Finalmente, se procedió a una etapa de análisis y el grupo investigador elaboró el documento final. Se resume todo el proceso en la figura 1.
Figura 1.
Metodología Delphi modificada.
Resultados
La totalidad de los participantes (19/19) respondió a las tres rondas Delphi.
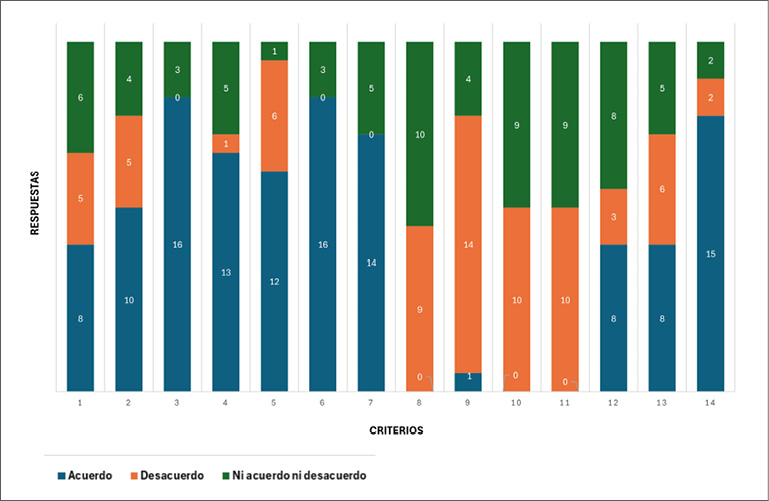
En la primera ronda, 4 de los 14 ítems fueron aceptados: no tener limitaciones para la actividad física; ausencia de exacerbaciones en el último año; mantenerse bien controlada con dosis bajas a demanda de corticoides inhalados (CI)/ formoterol o dosis bajas de CI + β2 adrenérgicos de acción corta (SABA, por sus siglas en inglés) según necesidad; espirometría con parámetros normales al inicio del tratamiento y/o después de tres meses de seguimiento. Fue descartado el criterio referido al recuento de eosinófilos en esputo. (Figura 2)
Figura 2.
Resultados de la primera ronda: criterios iniciales y nivel de consenso alcanzado.
1. Frecuencia de síntomas ≤ a 2 días por semana
2. Frecuencia de síntomas ≤ a 2 noches por mes
3. No tener limitaciones para la actividad física
4. Tener un ACT ≥ 20 puntos
5. Tener un ACQ 5 ≤ 1.5
6. Ausencia de exacerbaciones en el último año
7. Tener una espirometría normal al inicio y/o luego de tres meses de tratamiento
8. Tener un recuento elevado de eosinófilos en sangre
9. Tener un recuento de eosinófilos en esputo
10. Tener un dosaje elevado de IgE
11. Tener niveles de FENO elevados
12. Esperar un periodo de tiempo de al menos 3 meses para considerar al asma como leve
13. Usar SABA como rescate menor o iguala 2 canisters al año
14. Mantenerse bien controlada con dosis bajas de CI-formoterol o dosis bajas de CI + SABA según necesidad
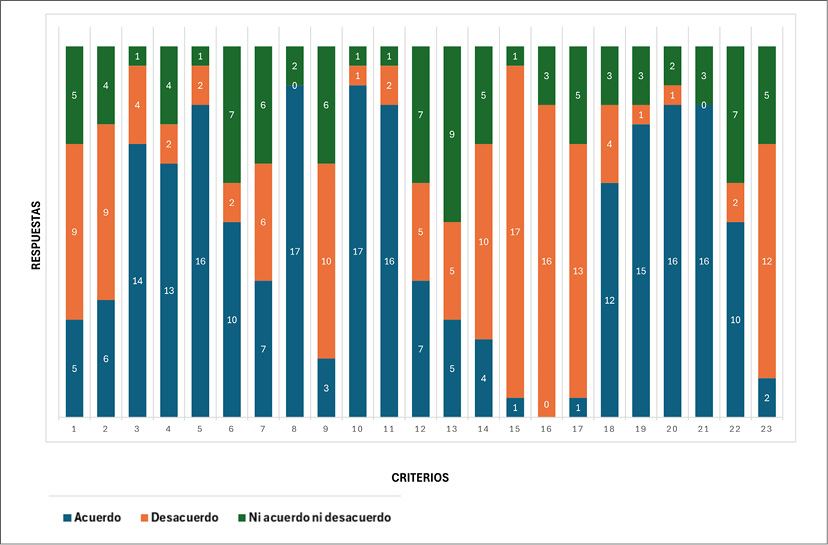
A partir de la pregunta abierta, se agregaron 13 criterios sugeridos por los expertos, que sumaron un total de 22 y fueron puestos a consideración en la segunda ronda. En esta, siete criterios fueron aceptados: frecuencia de síntomas diurnos o nocturnos por asma no mayor a 2 veces por mes; tener un puntaje en el Test de Control de Asma (ACT) ≥ 20 puntos; ausencia de ausentismo laboral y/o escolar; nunca haber presentado episodios de asma casi fatal, paro respiratorio o internación en unidad de terapia intensiva (UTI); no haber estado internado en sala general por asma en el último año; mantenerse bien controlada con dosis bajas de CI; no uso de corticoides sistémicos el último año. Dos criterios fueron descartados: tener un recuento elevado de eosinófilos en sangre; tener un dosaje elevado de IgE. (Figura 3)
Figura 3.
Resultados de la segunda ronda: criterios ampliados y nivel de consenso alcanzado.
1. Frecuencia de síntomas diurnos ≤ a 2 veces por semana
2. Frecuencia de síntomas ≤ a 2 noches por mes
3. Frecuencia de síntomas diurnos o nocturnos por asma no mayor a 2 veces por mes
4. No experimentar despertares nocturnos por asma más de 1 vez al mes
5. Tener un Score de ACT ≥ 20 puntos
6. Tener un Score ACQ 5 ≤ a 1
7. Tener un Score ACQ 5 ≤ a 1.5
8. Ausencia de ausentismo laboral y escolar
9. Comprende a pacientes que solo presentan síntomas de asma relacionados con el ejercicio
10. No haber presentado nunca episodios de asma casi fatal, paro respiratorio o internación en UTI
11. No haber estado internado en sala general por asma en el último año
12. No tener antecedentes de tabaquismo, enfermedad psiquiátrica que pueda afectar el manejo del asma o problemas de adherencia al tratamiento
13. Ausencia de comorbilidades, fundamentalmente las relacionadas con mecanismos inflamatorios del tipo T2 elevado, que puedan afectar la condición del asma
14. Los parámetros de fenotipificación deben formar parte de la definición
15.Tener un recuento elevado de eosinófilos en sangre
16. Tener un dosaje elevado de IgE
17. Tener niveles de FeNO elevados
18. Usar SABA como rescate menor o igual a 2 canisters al año
19. Mantenerse bien controlada con dosis bajas a demanda de CI-formoterol o dosis bajas de CI + SABA utilizados no más de 2 veces por mes
20. Puede mantenerse bien controlada con dosis bajas de CI
21. No uso de corticoides sistémicos el último año
22. Esperar un periodo de tiempo de al menos 3 meses con tratamiento para considerar al asma como leve
23. El asma puede considerarse leve solamente cuando está en remisión
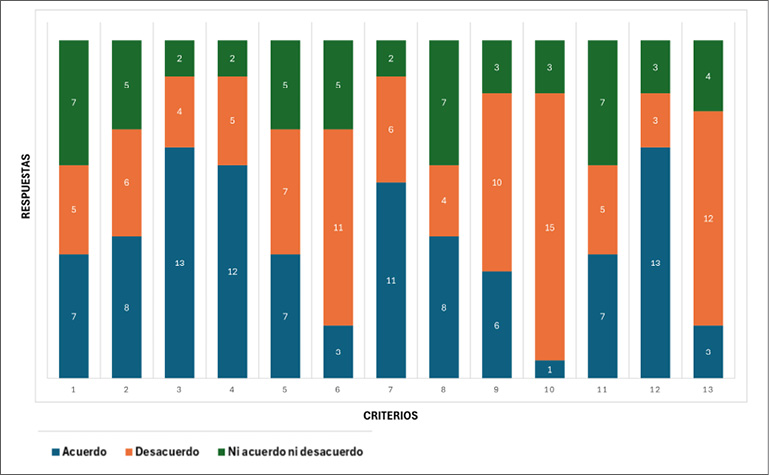
En la ronda final se descartó tener niveles elevados de fracción exhalada de óxido nítrico (FeNO). (Figura 4)
Figura 4.
Resultados de la tercera ronda: criterios finales y nivel de consenso alcanzado.
1. Frecuencia de síntomas diurnos ≤ a 2 veces por semana
2. Frecuencia de síntomas ≤ a 2 noches por mes
3. No experimentar despertares nocturnos por asma más de 1 vez al mes
4. Tener un Score ACQ 5 ≤ a 1
5.Tener un Score ACQ 5 ≤ a 1.5
6. Comprende a pacientes que solo presentan síntomas de asma relacionados con el ejercicio
7. No tener antecedentes de tabaquismo, enfermedad psiquiátrica que pueda afectar el manejo del asma o problemas de adherencia al tratamiento
8. Ausencia de comorbilidades, fundamentalmente las relacionadas con mecanismos inflamatorios del tipo T2 elevado, que puedan afectar la condición del asma
9. Los parámetros de fenotipificación deben formar parte de la definición.
10. Tener niveles de FeNO elevados
11. Usar SABA como rescate menor o igual a 2 canisters al año
12. Esperar un periodo de tiempo de al menos 3 meses con tratamiento para considerar al asma como leve
13. El asma puede considerarse leve solamente cuando está en remisión
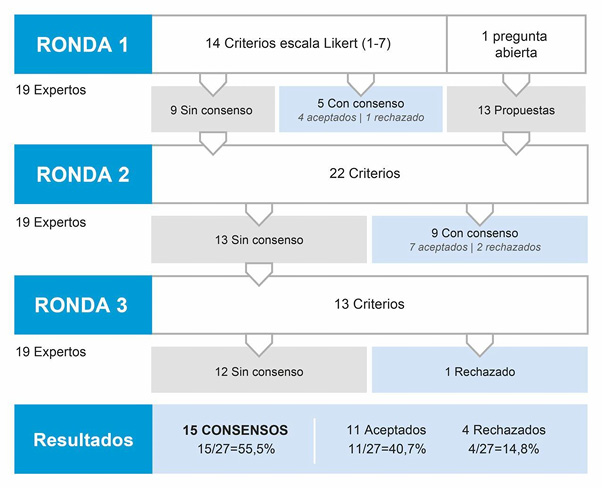
Se reseñan los resultados del proceso Delphi. (Figura 5)
Figura 5.
Resultados de las distintas etapas del proceso Delphi.
En la reunión plenaria, un grupo opinó que la presencia de síntomas de asma dos o más noches por mes descartaría que la patología fuera leve, debido a que el despertar sugiere una magnitud considerable de los síntomas. Se consideró preferir el ACT por sobre el Cuestionario de Control de Asma (ACQ) por ser su uso más común en nuestro medio. Sin embargo, dado que los cuestionarios que valoran síntomas clínicos deben ser simples, la aplicación de ambos se reservaría para contextos de atención especializada ya que resultan poco prácticos en el primer nivel. Finalmente, ninguna de estas escalas se incluyó en la definición.
Un aspecto considerado relevante en el plenario fue el de las comorbilidades y exposiciones. Su presencia dificulta el control y puede conducir a exacerbaciones, lo que exigiría niveles de tratamiento mayores que los del asma leve. Las comorbilidades consideradas más importantes fueron la obesidad, las relacionadas con la inflamación T2 alto (ej. rinosinusitis crónica), los trastornos psiquiátricos que dificultan la adherencia y la exposición al tabaco.
Respecto de las exacerbaciones, se aceptó que su ausencia en el último año y no haber tenido asma casi fatal, paro respiratorio o internación en UTI, son requisitos necesarios para considerar al asma como leve. Haber estado internado en sala por asma fue postulado como un indicador en contra de la naturaleza leve de la afección.
Se presenta el resultado final del consenso con definición y recomendaciones en la Tabla 2.
Tabla 2.
Definición consensuada de asma leve.
|
El asma se considera leve cuando los pacientes en tratamiento con dosis bajas de mantenimiento de CI, o bien dosis bajas de CI/SABA según necesidad, o dosis bajas de CI/formoterol según necesidad, logran control caracterizado por: |
|
|
|
|
|
|
Quedan excluidos quienes, a pesar de cumplir con los criterios previamente señalados, presentan:
|
|
Se recomienda: • No utilizar SABA como monoterapia en ningún caso de asma leve. • Asegurar que los pacientes con asma leve permanezcan bajo un régimen de tratamiento y seguimiento. |
Discusión
En este consenso, se buscó obtener una definición de asma leve simple y aplicable en la vida real por quienes asisten a estos pacientes. Al mismo tiempo, debería ser tan rigurosa que permitiera, a largo plazo, modificar factores que inciden en la morbimortalidad, tales como clasificación y tratamiento inadecuados, falta de mediciones objetivas y de pautas de alarma, ausencia de evaluaciones de riesgo de caída de la función pulmonar, exacerbación y muerte. Surgió con base en criterios seleccionados por médicos con amplios antecedentes en el campo asistencial y científico, que pertenecen a distintas regiones del país, y por consiguiente conocen la realidad de las mismas.
La definición alcanzada es retrospectiva ya que se basa en el tratamiento necesario para alcanzar el control y agrega criterios de exclusión y recomendaciones para el manejo de este grupo de pacientes, como se describe en detalle en la Tabla 2. El tratamiento coincide con los escalones 1 y 2 de los senderos preferido y alternativo de la Iniciativa Mundial para el asma (GINA, por sus siglas en inglés): dosis bajas de mantenimiento de CI, o bien dosis bajas de CI/SABA según necesidad, o dosis bajas de CI/formoterol según necesidad. (Tabla 3) En el plenario, se enfatizó en contra del uso de SABA sin CI, dado que puede acarrear un deterioro de la función pulmonar y un incremento en el riesgo de exacerbaciones y muerte. En el futuro inmediato, se prevé la disposición en el mercado de asociaciones fijas de budesonida-SABA que podrían ser alternativas a CI-formoterol.
Tabla 3.
Dosis bajas de corticoides inhalados (solos o en asociación) disponibles en Argentina. Adaptado de GINA (1), GEMA (2).
|
DROGA |
DOSIS BAJAS (µg/día) |
|---|---|
|
Budesonida (DPI) |
200 - 400 |
|
Propionato de fluticasona (pMDI/DPI) |
100 – 250 |
|
Furoato de fluticasona (DPI) |
92 |
|
Dipropionato de beclometasona (pMDI)* |
200 - 500 |
|
Furoato de mometasona (DPI)** |
62,5 |
DPI: inhalador de polvo seco, pMDI: inhalador presurizado de dosis medidas. * Partículas estándar. ** Breezhaler.
La Japanese Guidelines for Adult Asthma (JGL) clasifica prospectivamente la severidad del asma, es decir, sin tratamiento previo, pero sus puntos de corte clínicos son diferentes a los de este trabajo.16 Coincide con nuestra definición en incluir parámetros funcionales, como una espirometría con FEV1 ≥80%, aunque agrega la variación diaria de pico flujo espiratorio (PEF) entre 20 y 30%, poco utilizada en nuestro medio en la actualidad.
En este estudio, se considera que la espirometría debe estar dentro de los parámetros de referencia al inicio del tratamiento y/o después de tres meses de seguimiento. No es reemplazable por cuestionarios como el ACT. En un artículo de validación del ACT en español, se encontró una correlación débil de este indicador con el FEV1 y con la severidad.19 Un 40% de los pacientes con FEV1 menor al 60% respondió tener su asma bien o totalmente controlada en el ACT.19 La espirometría es una medida objetiva y su seguimiento longitudinal permite valorar el riesgo de caída anual de la función pulmonar. Es conveniente destacar que las escalas numéricas de control de síntomas no están validadas para el uso de CI-LABA o CI-SABA como medicación de rescate o estrategia anti-inflammatory reliever (AIR) de GINA.1
El control del asma incluye además el riesgo de exacerbaciones. La bibliografía discute si el asma leve lo sigue siendo cuando tiene riesgo alto. Uno de los expertos de nuestro consenso (LJN) se refirió a la combinación de palabras “asma” y “leve” como un “oxímoron”, figura retórica que designa a dos elementos que se contradicen. La calificación de “leve” no debiera resultar tranquilizadora ni eximir de realizar el tratamiento y seguimiento de los pacientes.
En este sentido, la guía GINA, en su actualización 2025, discute el uso del término leve por la posibilidad de ocultar este aspecto y llevar al uso inapropiado de SABA sin CI.1 La guía sugiere que el término “leve”, aunque no puede eliminarse, en lo posible debe ser evitado.1 Por su parte, la guía BTS/NICE/SIGN 2024 propone una atención estratificada por el riesgo, en la que los pacientes son identificados por alertas en sistemas informáticos de los médicos generalistas.20 En el mismo sentido, Mohan et al. subclasifican esta variante del asma en cuatro grupos según el riesgo de exacerbaciones y de caída de la función pulmonar.21 Para estos autores, el grupo D, con nivel alto tanto de síntomas como de riesgos, debería quedar afuera del rótulo de “leve”.21 El nivel de complejidad de esta subclasificación no la hace aplicable en la vida diaria, pero tiene el valor de poner en foco el tema. Jenkins et al proponen diferenciar asma leve como de bajo y alto riesgo; la de bajo riesgo no debería tener exacerbaciones ni despertares nocturnos en los últimos dos años.22
En cuanto a los biomarcadores, si bien fueron rechazados por ser el objeto de este trabajo alcanzar una definición a aplicar en todos los niveles de atención, se discutió el posible rol de los eosinófilos en sangre ya que se trata de una medición ampliamente disponible. Descartadas otras causas, la eosinofilia con un punto de corte de 200 células/µL se asocia con exacerbaciones de asma, en tanto que un número ≥ 400 células/µL es un predictor aún más fuerte.23 Sin embargo, no resulta exigible para nuestra definición. La medición del FeNO es sencilla, pero el equipo solo está disponible en pocos centros en el país.
La participación en el plenario fue del 84% de los expertos, una cifra robusta dado el carácter sincrónico de la reunión, lo que es una fortaleza del trabajo. Se discutió en esta instancia un aspecto considerado muy relevante como el de las comorbilidades y las exposiciones. El grupo investigador consensuó en equiparar la exposición al e-cigarrillo a la del cigarrillo convencional. La naturaleza modificable de la mayoría de estas comorbilidades y exposiciones implica que, al abordarlas con intervenciones terapéuticas adecuadas, se podría lograr un mejor control. Así, al considerar estas condiciones como “rasgos tratables”, su manejo exitoso podría llevar a una reevaluación de la severidad y permitir que el asma pase a la categoría leve.
A la definición obtenida, se agregaron las recomendaciones de no utilizar SABA como monoterapia y asegurar que los pacientes con asma leve reciban control médico regular, al igual que las formas más severas de la enfermedad. La mortalidad por asma en sus diversas severidades interpela a la comunidad médica y es uno de los motivos de nuestra preocupación. En Argentina, hubo 44 muertes en el grupo etario de 5 a 39 años en el período 1980-2013, en su mayoría evitables.24 La tasa bruta y ajustada fue de 0,19 muertes por 100.000 habitantes para el bienio 2014-2015.24 En el período 2020-2023, se registraron 17 muertes en menores de 20 años, según la Dirección de Estadísticas e Información de Salud del Ministerio de Salud de la Nación, Argentina. Se consideró que la prescripción de SABA sin CI es un factor relevante en el mantenimiento de esta situación.
Nuestro consenso rechazó un criterio propuesto por uno de los expertos referido a que “solo el asma en remisión puede considerarse leve”. Menzies-Gow et al. realizaron un consenso Delphi en el que aceptan que, al igual que en artritis reumatoidea, colitis ulcerosa, enfermedad de Crohn y lupus eritematoso sistémico, “la remisión en asma debería aplicarse a todos los niveles de severidad de la enfermedad”.25 Las guías GINA y GEMA 5.5 incorporan a la remisión clínica como objetivo terapéutico principal.1,2
La necesidad de no encubrir el asma con riesgo futuro bajo el rótulo de leve determina un punto fuerte de nuestra definición. Recientemente, han surgido herramientas que permitirían valorar el control actual de síntomas y algunos aspectos del riesgo de futuras exacerbaciones como el Cuestionario sobre la afectación y el riesgo en asma (Asthma Impairment and Risk Questionnaire, AIRQ), que consta de 10 ítems en una escala de 0 a 10 e incluye los aspectos de control actual (síntomas) y de los últimos 12 meses (exacerbaciones). El AIRQ está validado en idioma español.26
La mayoría de estos asmáticos son asistidos en el primer nivel de atención, de manera que la calidad de vida relacionada con la enfermedad dependerá del control que puedan alcanzar en esta instancia, con el tratamiento correcto. Es pues crucial la difusión de los conceptos aquí expuestos entre clínicos y generalistas para alcanzar a la mayor población posible de pacientes. El especialista, por su parte, podrá usar otras herramientas como cuestionarios más sofisticados, medición de FeNO u otros biomarcadores si lo considera. En última instancia, se espera que su proceder termine por impregnar la práctica de los otros niveles mediante la docencia, referencia y contrarreferencia.
El trabajo tiene una serie de limitaciones. En relación con el método Delphi, las respuestas de los expertos pueden ser hasta cierto punto subjetivas ya que dependen de su experiencia y prejuicios. Además, la opinión de los pacientes sobre cómo interpretan el término “leve” aplicado a su propia enfermedad fue excluida. No obstante, creemos que la definición obtenida resulta de utilidad para los pacientes, los médicos generalistas e investigadores.
Conclusiones
Se elaboró una definición consensuada, operativa, accesible y simple, aplicable en atención primaria y, eventualmente, en el ámbito de los especialistas. Se consideró al asma como leve cuando los pacientes en tratamiento con dosis bajas de mantenimiento de CI, o bien dosis bajas de CI/SABA según necesidad, o dosis bajas de CI/formoterol según necesidad, logran control: síntomas diurnos menores o iguales a dos veces por semana, síntomas nocturnos menores o iguales a una vez por mes, ausencia de limitaciones para la realización de actividades físicas, ausencia de exacerbaciones en el último año y espirometría normal al inicio del tratamiento y/o después de tres meses de seguimiento. Deja de considerarse leve si, a pesar de cumplir con los criterios previamente señalados, los pacientes presentan antecedentes de asma casi fatal, paro respiratorio, internación en UTI, hospitalización en sala, tabaquismo activo, enfermedades psiquiátricas o asma durante el embarazo. Asimismo, hubo acuerdo en el tipo de tratamiento necesario para lograr el control, resaltando la inconveniencia de usar cualquier terapéutica que no contenga CI. Si bien se discute la pertinencia del término leve para los pacientes que reúnen las condiciones mencionadas, la denominación debiera seguir vigente hasta tanto se encuentre otra expresión más apropiada para poder identificar a estos enfermos.
Agradecimientos: Expertos: Juan Pablo Casas; Daniel Colodenco; Ricardo del Olmo; Pedro Carlos Elías; Ricardo Gené; Eduardo Giugno; Ana María López; Martín Maillo; Walter Matarucco; Luis Nannini; Daniel Pascansky; Miguel Penizzotto; Ramón Rojas; Eduardo Schiavi; Daniel Schönfeld; Martín Sivori; Ana María Stok; Sebastián Wustten; Ignacio Zabert. Asesoramiento y estadística: Marina Khoury; Juan Carlos Bossio; Sergio Arias. Asociación Argentina de Medicina Respiratoria (AAMR) Asistencia técnica: Horacio Luis Márquez. Gráficos: Ailín Carlés.
Financiamiento: los autores declaran que el trabajo no tuvo financiamiento.
Conflictos de interés: los autores declaran no tener conflictos de interés en relación con la elaboración y contenido de este trabajo.
Declaración de cumplimiento ético: todos los participantes otorgaron su consentimiento informado para cada encuesta, además toda la información proporcionada se mantuvo confidencial y anónima.
Contribuciones de los autores: todos los autores contribuyeron en la elaboración del trabajo y en la revisión final del texto, aprobaron la versión final y asumen responsabilidad por el contenido del manuscrito.
Los Editores en Jefe, Dres. Carlos Luna y Francisco Arancibia, realizaron el seguimiento del proceso de revisión y aprobaron este artículo.
Referencias
1. Global Initiative for Asthma. Global strategy for asthma management and prevention, 2025. [Internet]. [Consultado 1 jun 2025]. Disponible en: www.ginasthma.org
2. Sociedad Española de Neumología y Cirugía Torácica. GEMA 5.4 Guía Española para el manejo del asma, 2024. [Internet]. [Consultado 1 jun 2025]. Disponible en: www.gemasma.com
3. Vos T, Abajobir AA, Abbafati C, Abbas KM, Abbate KH, Abd-Allah F et al. Global, regional, and national incidence, prevalence, and years lived with disability for 328 diseases and injuries for 195 countries, 1990–2016: a systematic analysis for the Global Burden of Disease Study 2016. Lancet 2017;390(10100):1211-1259. https://doi.org/10.1016/S0140-6736(17)32154-2
4. Rabe APJ, Loke WJ, Gurjar K, Brackley A, Lucero-Prisno III DE. Global Burden of Asthma, and Its Impact on Specific Subgroups: Nasal Polyps, Allergic Rhinitis, Severe Asthma, Eosinophilic Asthma. J Asthma Allergy 2023;16:1097-1113. https://doi.org/10.2147/JAA.S418145
5. Ministerio de Salud de la Nación. Guía de Práctica Clínica Nacional sobre Tratamiento del Asma Leve en Personas Adultas, 2022. Argentina. [Internet]. [Consultado 1 jun 2025]. Disponible en: https://www.boletinoficial.gob.ar/detalleAviso/primera/298286/20231113
6. Arias SJ, Neffen H, Bossio JC, Calabrese CA, Videla AJ, Armando GA et al. Prevalence and Features of Asthma in Young Adults in Urban Areas of Argentina. Arch Bronconeumol 2018;54(3):134–9. https://doi.org/10.1016/j.arbres.2017.08.021
7. Dusser D, Montani D, Chanez P, de Blic J, Delacourt C, Deschildre A et al. Mild asthma: an expert review on epidemiology, clinical characteristics and treatment recommendations. Allergy 2007;62(6):591-604. https://doi.org/10.1111/j.1398-9995.2007.01394.x
8. Chapman KR. Impact of ‘mild’ asthma on health outcomes: findings of a systematic search of the literature. Respir Med 2005;99(11):1350-62. https://doi.org/10.1016/j.rmed.2005.03.020
9. Mohan A, Ludwig A, Brehm C, Lugogo NL, Sumino K, Hanania NA. Revisiting Mild Asthma: Current Knowledge and Future Needs. Chest 2022;161(1):26-39. https://doi.org/10.1016/j.chest.2021.09.004
10. Domingo C, García G, Gemicioglu B, Vu-Van G, Larenas-Linnemann D, Neffen H. Consensus on mild asthma management: results of a modified Delphi study. J Asthma 2023;60(1):145-157. https://doi.org/10.1080/02770903.2022.2034850
11. FitzGerald JM, Barnes PJ, Chipps BE, Jenkins CR, O’Byrne PM, Pavord ID et al. The burden of exacerbations in mild asthma: a systematic review. ERJ Open Res 2020;6(3):00359-2019. https://doi.org/10.1183/23120541.00359-2019
12. Mohan A, Lugogo NL, Hanania NA, Reddel HK, Akuthota P, O’Byrne PM et al. Questions in Mild Asthma: An Official American Thoracic Society Research Statement. Am J Respir Crit Care Med 2023;207(11):e77-e96. https://doi.org/10.1164/rccm.202304-0642ST
13. Levy ML. The national review of asthma deaths: what did we learn and what needs to change? Breathe (Sheff) 2015;11(1):14-24. https://doi.org/10.1183/20734735.008914
14. National Institute for Health and Care Excellence (NICE). Asthma: diagnosis, monitoring and chronic asthma management. London, 2021. [Internet]. [Consultado 1 jun 2025]. Disponible en: https://www.ncbi.nlm.nih.gov/books/NBK560178/pdf/Bookshelf_NBK560178.pdf
15. Cloutier MM, Baptist AP, Blake KV, Brooks EG, Bryant-Stephens T, DiMango E et al. Expert Panel Working Group of the National Heart, Lung, and Blood Institute (NHLBI) administered and coordinated National Asthma Education and Prevention Program Coordinating Committee (NAEPPCC). 2020 Focused Updates to the Asthma Management Guidelines: A Report from the National Asthma Education and Prevention Program Coordinating Committee Expert Panel Working Group. J Allergy Clin Immunol 2020;146(6):1217-1270. https://doi.org/10.1016/j.jaci.2020.10.003
16. Niimi A, Fukunaga K, Taniguchi M, Nakamura Y, Tagaya E, Horiguchi T et al. Executive summary: Japanese guidelines for adult asthma (JGL) 2021. Allergol Int 2023;72(2):207-226. https://doi.org/10.1016/j.alit.2023.02.006
17. Yang CL, Hicks EA, Mitchell P, Reisman J, Podgers D, Hayward KM et al. 2021 Canadian Thoracic Society Guideline A focused update on the management of very mild and mild asthma. Can J Resp Crit Care Sleep Med 2021;5(4):205–245. https://doi.org/10.1080/24745332.2021.1877043
18. Schifano J, Niederberger M. How Delphi studies in the health sciences find consensus: a scoping review. Syst Rev 2025;14(1):14. https://doi.org/10.1186/s13643-024-02738-3
19. Rodrigo GJ, Arcos JP, Nannini LJ, Gonzalez-Broin M, Contrera M, Piñeyro L et al. Reliability and factor analysis of the Spanish version of the asthma control test. Ann Allergy Asthma Immunol 2008;100(1):17-22. https://doi.org/10.1016/S1081-1206(10)60399-7
20. British Thoracic Society (BTS); National Institute for Health and Care Excellence (NICE); Scottish Intercollegiate Guidelines Network (SIGN). BTS/NICE/SIGN joint guideline on asthma: diagnosis, monitoring and chronic asthma management (November 2024) - summary of recommendations. Thorax 2025;thorax-2024-222910. https://doi.org/10.1136/thorax-2024-222910
21. Mohan A, Lugogo NL. Mild asthma: Lessons learned and remaining questions. Respir Med 2023;216:107326. https://doi.org/10.1016/j.rmed.2023.107326
22. Jenkins CR. Mild asthma: Conundrums, complexities and the need to customize care. Respirology 2024;29(2):94-104. https://doi.org/10.1111/resp.14646
23. Mallah N, Rodriguez-Segade S, Gonzalez-Barcala FJ, Takkouche B. Blood eosinophil count as predictor of asthma exacerbation. A meta-analysis. Pediatr Allergy Immunol 2021;32(3):465-478. https://doi.org/10.1111/pai.13403
24. Ministerio de Salud de la Argentina. Administración Nacional de Laboratorios e Institutos de Salud (ANLIS) “Carlos G. Malbrán”. Instituto Nacional de Enfermedades Respiratorias (INER) “Emilio Coni”. Mortalidad por Asma de 5 a 39 Años en Argentina: 1980-2013. 2015. [Internet]. [Consultado 1 jun 2025]. Disponible en: https://www.argentina.gob.ar/sites/default/files/iner_asma_3_-_mortalidad-por-asma-de-5-a-39-anos-en-argentina-1980-2015.pdf
25. Menzies-Gow A, Bafadhel M, Busse WW, Trudo F, Fageras M, Ambrose CS et al. An expert consensus framework for asthma remission as a treatment goal. J Allergy Clin Immunol 2020;145(3):757-765. https://doi.org/10.1016/j.jaci.2019.12.006
26. Pérez de Llano L, Martínez Moragón E, Entrenas LM, Martínez Rivera C, Cisneros C, Blanco-Aparicio M et al. Validation of the Asthma Impairment and Risk Questionnaire (AIRQ) in Spain: a useful tool to assess asthma control in adolescent and adult patients. J Investig Allergol Clin Immunol 2023;33(5):397-400. https://doi.org/10.18176/jiaci.0881