
Caso Clínico | Respirar, 2026; 18 (1): 212-217 | ISSN 2953-3414 | https://doi.org/10.55720/respirar.18.1.17
Enfermedad de Goodpasture, un diagnóstico alternativo
Goodpasture’s Disease, an Alternative Diagnosis
Universidad de Buenos Aires, Hospital de Clínicas José de San Martín, División Neumonología, Ciudad Autónoma de Buenos Aires, Argentina.
Sanatorio Anchorena Recoleta, Ciudad Autónoma de Buenos Aires, Argentina.
Autor corresponsal:
Besteiro Guillermo. E-mail: dr.guillermobesteiro@gmail.com
RECIBIDO:
16 julio 2025
APROBADO:
15 octubre 2025
Resumen
Introducción: La enfermedad de Goodpasture es una patología con base autoinmune, mediada por anticuerpos anti membrana basal glomerular (MBG). La afectación es principalmente renal y/o pulmonar. Es poco frecuente y puede ser grave e incluso mortal si no se arriba al diagnóstico temprano.
Presentación del caso: Paciente con síndrome febril asociado a tos seca y astenia, recibió antibioticoterapia ambulatoria sin mejoría. Se estudió con múltiples tomografías de tórax que evidenciaron imágenes nodulares migratorias y perfil reumatológico negativo. Lavado bronquioalveolar sin desarrollo de gérmenes, punción percutánea y biopsia por videotoracoscopía con patrón inflamatorio de la muestra, sin atipía. Evolucionó con hemoptisis. Se solicitaron anticuerpos anti membrana basal glomerular que resultaron positivos, por lo que se interpretó el cuadro como enfermedad de Goodpasture.
Discusión: La enfermedad de Goodpasture es una entidad poco frecuente. Los anticuerpos anti MBG pueden afectar tanto a los riñones, causando glomerulonefritis rápidamente progresiva, como a los pulmones dando hemorragia alveolar, principalmente. Entre el 60 y el 80% de los pacientes tienen manifestaciones clínicamente evidentes de enfermedad pulmonar/renal y menos del 10% tienen enfermedad limitada a los pulmones.
Conclusión: La enfermedad de Goodpasture con afectación únicamente pulmonar es una entidad infrecuente, puede simular otras patologías y volverse un desafío. Al ser poco prevalente, el tiempo hasta el diagnóstico es mayor y, por lo tanto, conlleva a un retraso en el tratamiento dirigido de la patología.
Palabras clave: enfermedad de Goodpasture; nódulos migratorios; anticuerpos anti membrana basal glomerular.
Abstract
Introduction: Goodpasture’s disease is an autoimmune disease mediated by anti-glomerular basement membrane (GBM) antibodies. It primarily affects the kidneys and/or lungs. It is rare and can be severe and even fatal if not diagnosed early.
Case presentation: A patient with febrile syndrome associated with a dry cough and asthenia received outpatient antibiotic therapy without improvement. Multiple chest CT scans revealed migratory nodular images and a negative rheumatologic profile. Bronchoalveolar lavage revealed no germ development, and percutaneous puncture and video-assisted thoracoscopic biopsy revealed an inflammatory pattern in the sample, without atypia. The patient developed hemoptysis. Anti-glomerular basement membrane antibodies were requested, which were positive, interpreting the condition as Goodpasture’s disease.
Discussion: Goodpasture’s disease is a rare entity. Anti-GBM antibodies can affect both the kidneys, causing rapidly progressive glomerulonephritis, and the lungs, primarily causing alveolar hemorrhage. Between 60% and 80% of patients have clinically evident manifestations of lung/kidney disease, and less than 10% have disease limited to the lungs.
Conclusion: Goodpasture’s disease, which affects only the lungs, is a rare entity and can mimic other pathologies and become a challenge. Because it is relatively uncommon, the time to diagnosis is longer, leading to a delay in targeted treatment.
Key words:Goodpasture’s disease; migratory nodules; anti-glomerular basement membrane antibodies.
Introducción
La enfermedad de Goodpasture es una enfermedad con características autoinmunes asociada a anticuerpos dirigidos contra antígenos de la membrana basal glomerular (MBG) presente en órganos específicos como los riñones y pulmones.1 Estos anticuerpos pueden provocar glomerulonefritis rápidamente progresiva (GNPR) o hemorragia pulmonar debido a las similitudes del colágeno en la membrana basal.3
Es poco frecuente en la población general, con una incidencia de 1 por cada 2 millones de personas al año. El síndrome tiene una distribución por edad bimodal alrededor de la tercera y sexta décadas de la vida. Cabe destacar que los pacientes más jóvenes tienen mayor probabilidad de presentar afectación pulmonar, mientras que los pacientes mayores tienen mayor probabilidad de presentar enfermedad renal menos grave.
La semiología respiratoria suele ser inespecífica y los pacientes pueden manifestar desde disnea, tos crónica, hasta hemoptisis.
El tratamiento estándar consiste en una terapia combinada de plasmaféresis, prednisolona y ciclofosfamida.3
Caso clínico
Paciente femenina de 59 años con antecedentes de ex tabaquista de 20 paquetes año, EPOC Gold 2 B, neumonías a repetición, bypass gástrico, alérgica a ampicilina y sulfonamidas. Padre fallecido de cáncer de pulmón. Consultó al servicio de urgencias por tos seca, disnea clase funcional II y registros subfebriles de 5 días de evolución. Le realizaron test para SARS-CoV-2 con resultado negativo y le indicaron tratamiento sintomático. Luego de una semana volvió a consultar por la persistencia de los síntomas y agregó fiebre de hasta 38, 5°C. La radiografía de tórax evidenció una opacidad en la base pulmonar derecha, por lo que fue medicada con claritromicina. Luego de una semana, la paciente persistió febril y le adicionaron levofloxacina. Tras cumplir el tratamiento antibiótico, no hubo mejoría del cuadro clínico por lo que se decidió su hospitalización. La tomografía computada de tórax (TC) evidenció una opacidad de aspecto consolidativo de disposición yuxta cisural, de bordes irregulares y cavitación central que comprometía el segmento posterior del lóbulo superior derecho, opacidades pseudonodulares en lóbulo medio y árbol en brote comprometiendo extensamente el campo pulmonar derecho. (Figura 1) Los exámenes de laboratorio encontraron reactantes de fase aguda elevados, perfil reumatológico negativo e IgE elevada como datos a destacar. La función renal fue normal y las serologías negativas. Se realizó lavado bronquio alveolar (BAL) sin hallazgos patológicos.
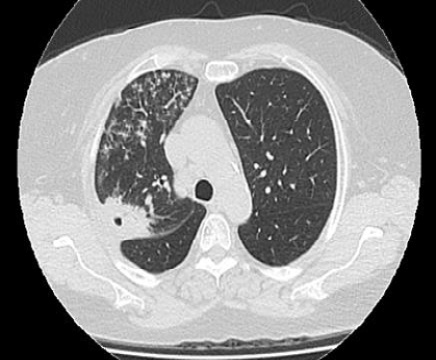
Figura 1.
Consolidación yuxta cisural, de bordes irregulares y cavitación central en el lóbulo superior derecho y árbol en brote comprometiendo el campo pulmonar derecho.
Por mejoría del cuadro clínico, se programó TC de tórax control al mes en la que se visualizaron dos imágenes nodulares a nivel de lóbulo superior derecho. (Figura 2) La punción percutánea con aguja fina de la lesión consolidativa nodular concluyó en la ausencia de atipias en la anatomía patológica, pero con marcadores tumorales TTF1, CK 7 y P63 positivos. Una nueva TC de tórax mostró franca mejoría de las imágenes nodulares previamente descritas, pero con la aparición de un nódulo de 15 mm en lóbulo inferior izquierdo. (Figura 3) Posteriormente, se decidió realizar biopsia quirúrgica por medio de una videotoracoscopía (VATS) de la lesión de la base pulmonar izquierda y la anatomía patológica informó un patrón inflamatorio inespecífico (ver exámenes complementarios).
Figura 2.
Imágenes nodulares a nivel de lóbulo superior derecho.
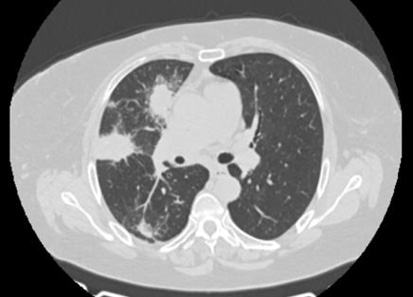
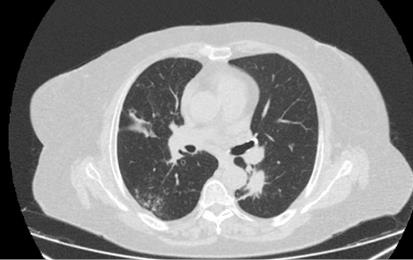
Figura 3.
Nódulo de 15 mm en lóbulo inferior izquierdo.
La paciente continuó con registros subfebriles diarios, marcada astenia y tos seca. Se interpretó el cuadro como posible neumonía organizativa y se inició tratamiento con meprednisona 40 mg al día. La paciente mejoró parcialmente, sin repetir eventos febriles; por lo que al mes de iniciado el tratamiento con corticoides, se comenzó su reducción. Durante el descenso, la paciente presentó hemoptisis moderada por lo que consultó nuevamente al servicio de emergencias. Los exámenes de laboratorio mostraron anemia de trastornos crónicos y reactantes de fase aguda elevados. Una nueva TC de tórax describió dos imágenes nodulares de bordes definidos, mayores a 15 mm, en lóbulo superior derecho y lóbulo medio. (Figura 4) Se escaló la dosis de meprednisona a 40 mg al día y se extendió el perfil reumatológico donde se obtuvo resultado de anticuerpos anti membrana basal glomerular que fueron positivos.
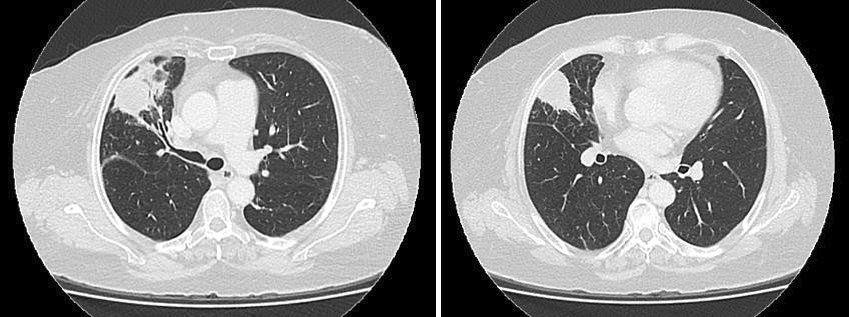
Figura 4.
Imágenes nodulares de bordes definidos mayores a 15 mm en lóbulo superior derecho y lóbulo medio.
Exámenes complementarios
Los principales resultados de laboratorio se describen en las Tablas 1 y 2. Por otra parte, el hisopado nasofaríngeo para SARS-CoV-2 y panel viral resultó negativo. Los hemocultivos fueron negativos y la reacción de Mantoux (PPD) anérgica. Los resultados del lavado bronquioalveolar se describen en la Tabla 3.
-Anatomía patológica de punción percutánea: células epiteliales y estromales con leves cambios reactivos, numerosos neutrófilos, macrófagos alveolares y hematíes.
-Anatomía patológica de VATS: focos de enfisema, leve infiltrado inflamatorio mononuclear y aislados acúmulos linfoides.
Tabla 1.
Exámenes de laboratorio general.
|
Hematocrito |
39% |
IgE |
509 UI/ml |
|
Hemoglobina |
11,8 g/L |
IgE anti-Aspergillus |
Negativa |
|
Leucocitos |
6600/mm3 |
IgG 4 |
Negativo |
|
Eosinófilos |
630/l |
LDH |
296 U/I |
|
Plaquetas |
235000/mm3 |
HIV |
Negativo |
|
Uremia |
35 mg/dl |
VDRL |
Negativo |
|
Creatininemia |
0,8 mg/dl |
Serologías hepatitis |
Negativas |
|
VSG |
70 mm/h |
Orina |
Proteínas + |
|
PCR |
5,4 mg/dl |
Ref.: VSG, eritrosedimentación; PCR, proteína C reactiva; LDH, láctico deshidrogenasa.
Tabla 2.
Resultado de exámenes de laboratorio inmunológicos.
|
FAN |
Negativo |
|
ANCA |
Negativo |
|
FR |
Negativo |
|
Ac. Anti SCL 70 |
Negativo |
|
Ac. Anti CCP |
Negativo |
|
Ac. Anti JO 1 |
Negativo |
|
Ac. Anto RO/LA |
Negativo |
|
Ac. Anti MBG |
Positivo |
Ref.: FAN (factor antinúcleo), ANCA (anticuerpos anti citoplasmáticos), FR (factor reumatoideo), MBG (membrana basal glomerular).
Tabla 3.
Resultados microbiológicos y fórmula del lavado bronco-alveolar.
|
Recuento diferencial |
-Macrófagos: 68% |
|
-Neutrófilos: 20% |
|
|
-Eosinófilos: 1% |
|
|
-Linfocitos: 10% |
|
|
-Células bronquiales: 1% |
|
|
-Células pavimentosas: 0% |
|
|
Directo y cultivos |
Negativos |
|
Células epiteliales |
< 1% |
|
Leucocitos |
0-1 por campo |
|
Monocitos – Macrófagos |
No se observan |
|
Tinción de Gram |
No se observan bacterias |
|
Tinción de Ziehl Neelsen |
Negativo |
Discusión
La enfermedad de Goodpasture con compromiso solo pulmonar es una enfermedad autoinmune que requiere un alto índice de sospecha clínica e imagenológica para arribar al diagnóstico. La hemorragia alveolar es la característica más frecuente en la tomografía de tórax.
Los anticuerpos pueden provocar daño pulmonar y/o renal debido a las similitudes del colágeno en la membrana basal.
Las pruebas de ELISA para anticuerpos anti-MBG presentan una alta sensibilidad (> 95%) y especificidad (>97%).6
Entre el 60 y el 80% de los pacientes tienen manifestaciones clínicamente evidentes de enfermedad pulmonar y renal, entre el 20 y el 40% tienen solo enfermedad renal y menos del 10% tienen enfermedad limitada a los pulmones.2
Las manifestaciones clínicas del Goodpasture pueden variar. En algunos pacientes, los síntomas respiratorios ocurren semanas o meses antes de que las manifestaciones renales sean evidentes. El síntoma más común es la hemoptisis que se acompaña de disnea continua o episódica, fatiga y tos que generalmente es aguda, pero en ocasiones es subaguda y recurrente.4
El factor determinante para la respuesta terapéutica y el diagnóstico a largo plazo de la enfermedad es el diagnóstico precoz para prevenir la nefropatía terminal. Por lo tanto, el tratamiento estándar consiste en una terapia combinada de plasmaféresis, prednisolona y ciclofosfamida.
Dentro de los diagnósticos diferenciales de la enfermedad de Goodpasture cabe mencionar la granulomatosis eosinofílica con poliangeítis, lupus eritematoso sistémico, crioglobulinemia y la hemosiderosis pulmonar.
Conclusión
La enfermedad de Goodpasture es una entidad con una baja incidencia, lo que lleva a una demora en su diagnóstico y tratamiento. La afectación únicamente pulmonar es infrecuente y puede simular otras enfermedades respiratorias. Esto actúa como un distractor, puede resultar en tratamientos inadecuados y puede aumentar la probabilidad de progresión e impacto renal.
Financiamiento: el autor declara que el trabajo no tuvo financiamiento.
Conflictos de interés: el autor declara que no tiene conflictos de intereses relacionados con el tema de esta publicación.
Declaración de cumplimiento ético: Confidencialidad de los datos: el autor declara que en este artículo no aparecen datos de pacientes. Consentimiento informado: el/la paciente proporcionó su consentimiento informado por escrito para la publicación de este caso clínico y de las imágenes asociadas.
El Editor en Jefe, Dr. Francisco Arancibia, realizó el seguimiento del proceso de revisión y aprobó este artículo.
Referencias
1. Dammacco F, Battaglia S, Gesualdo L, Racanelli V. Goodpasture's disease: A report of ten cases and a review of the literatura. Autoimmun Rev 2013;12:1101-1108. https://doi.org/10.1016/j.autrev.2013.06.014
2. Greco A, Rizzo MI, De Virgilio A, Gallo A, Fusconi M, Pagliuca G et al. Goodpasture's syndrome: a clinical update. Autoimmun Rev 2015;14(3):246-53. https://doi.org/10.1016/j.autrev.2014.11.006
3. Lahmer T, Heemann U. Anti-glomerular basement membrane antibody disease: a rare autoimmune disorder affecting the kidney and the lung. Autoimmun Rev 2012;12(2):169-73. https://doi.org/10.1016/j.autrev.2012.04.002
4. Otero ORR, Moragues MJR, Ávila OE, et al. Síndrome de Goodpasture: Un enfoque pulmonar. Neumol Cir Torax. 2006;65(4):178-185.
5. Frankel SK, Cosgrove GP, Fischer A, Meehan RT, Brown KK. Update in the diagnosis and management of pulmonary vasculitis. Chest. 2006 Feb;129(2):452-465. https://doi.org/10.1378/chest.129.2.452
6. Sinico RA, Radice A, Corace C, Sabadini E, Bollini B. Anti-glomerular basement membrane antibodies in the diagnosis of Goodpasture syndrome: a comparison of different assays. Nephrol Dial Transplant 2006;21(2):397-401. https://doi.org/10.1093/ndt/gfi230
7. Reggiani F, L'Imperio V, Calatroni M, Pagni F, Sinico RA. Goodpasture syndrome and anti-glomerular basement membrane disease. Clin Exp Reumatol 2023;41(4):964-974. https://doi.org/10.55563/clinexprheumatol/tep3k5
8. Ooi JD, Petersen J, Tan YH, Huynh M, Willett ZJ, Ramarathinam SH et al. Dominant protection from HLA-linked autoimmunity by antigen-specific regulatory T cells. Nature 2017;545(7653):243-247. https://doi.org/10.1038/nature22329
9. Yang R, Cui Z, Zhao J, Zhao MH. The role of HLA-DRB1 alleles on susceptibility of Chinese patients with anti-GBM disease. Clin Immunol 2009;133(2):245-50. https://doi.org/10.1016/j.clim.2009.07.005
10. Peto P, Salama AD. Update on antiglomerular basement membrane disease. Curr Opin Rheumatol 2011;23(1):32-7. https://doi.org/10.1097/BOR.0b013e328341009f