
Artículo Original | Respirar, 2026; 18 (1): 59-75 | ISSN 2953-3414 | https://doi.org/10.55720/respirar.18.1.4
Características clínicas, patológicas y moleculares de los pacientes con cáncer primario de pulmón atendidos en el centro de experticia en oncología torácica de la Fundación Neumológica Colombiana
Clinical, Pathological and Molecular Characteristics of Patients with Primary Lung Cancer who Attended the Thoracic Oncology Expert Center at Fundación Neumológica Colombiana
1 Universidad de La Sabana, Facultad de Medicina, Chía, Colombia.
2 Fundación Neumológica Colombiana, Centro de experticia en neumología oncológica, Oncotórax Rexpira, Bogotá, Colombia.
3 Fundación Neumológica Colombiana, Centro Internacional de Investigación en Neumología y Salud Respiratoria (CINEUMO), Bogotá, Colombia.
4 Universidad de La Sabana, Facultad de medicina, Departamento de Pediatría, Chía, Colombia.
5 Fundación Santafé de Bogotá, Departamento de Oncología, Bogotá, Colombia.
AUTOR CORRESPONSAL:
Lucia Catalina Silva Cala. E-mail: lsilva@neumologica.org
Recibido:
29 abril 2025
Aprobado:
22 agosto 2025
Resumen
Introducción: Los pacientes con cáncer de pulmón han sido poco caracterizados en Colombia.
Métodos: Este estudio de corte transversal describe los pacientes con cáncer primario de pulmón no hematolinfoide atendidos en el centro de experticia en oncología torácica de la Fundación Neumológica Colombiana entre enero de 2019 y agosto de 2023. Se evaluaron características demográficas, factores de riesgo, comorbilidades, función pulmonar, histología, estadio, y tiempo al diagnóstico y al tratamiento. Adicionalmente, en aquellos con carcinomas pulmonares de célula no pequeña (CPCNP), se evaluó perfilamiento genómico y expresión de PD-L1.
Resultados: De 163 pacientes con cánceres primarios pulmonares, 59,5% eran mujeres y 49,7% no tenían historia de consumo de cigarrillo, 41,7% tenían alguna comorbilidad cardiopulmonar. Los CPCNP fueron 88,3%, los tumores neuroendocrinos 6,7% y los carcinomas neuroendocrinos 4,3%. El 31,2% de los CPCNP fueron estadio I o II y 43,1% fueron estadio IV. Se encontraron mutaciones accionables en 51,9% (42/81) de los pacientes con CPCNP evaluados para al menos una mutación; las más frecuentes fueron mutaciones de EGFR encontradas en 42,0% (34/81). La mediana de tiempo al diagnóstico fue de 54 días y al tratamiento de 46 días.
Conclusiones: El sexo femenino, la ausencia de historia de consumo de cigarrillo y las mutaciones accionables fueron más frecuentes que lo reportado en estudios previos en Colombia. El tiempo hasta el diagnóstico y el tratamiento fue más prolongado que lo estimado por los organismos oficiales nacionales.
Palabras clave: estudios transversales; neoplasias de pulmón; comorbilidad; pruebas genéticas; diagnóstico retrasado; retraso del tratamiento.
Abstract
Introduction: Lung cancer patients have rarely been characterized in Colombia.
Methods: This cross-sectional study describes all patients with non-hematolymphoid primary lung malignancies who attended the thoracic oncology expert center at Fundación Neumológica Colombiana between January 2019 and August 2023. Demographics, risk factors, comorbidities, lung function, histology, staging, and time to diagnosis and treatment were evaluated. Additionally, genomic profiling and PD-L1 expression were assessed in patients with Non-Small Cell Lung Cancer (NSCLC).
Results: Of 163 patients with primary lung cancer, 59.5% were women and 49.7% had no history of tobacco consumption. 41.7% had a cardiopulmonary comorbidity. NSCLC accounted for 88.3%, neuroendocrine tumors 6.7% and neuroendocrine carcinomas 4.3%. 31.2 % of NSCLC were stage I or II and 43.1 % were stage IV. A targetable mutation was found in 51.9% (42/81) of patients with NSCLC tested for at least one of them. EGFR mutations were found in 42.0% (34/81) of patients tested, making it the most frequent targetable mutation. The median time to diagnosis was 54 days and to treatment was 46 days.
Conclusions: Female sex, absence of tobacco consumption history and targetable mutations were more frequent than previously reported in Colombia. The time to diagnosis and treatment was longer than estimated by local government agencies.
Keywords: cross-sectional studies; lung neoplasms; comorbidity; genetic testing; delayed diagnosis; treatment delay.
Introducción
El cáncer de pulmón es el más letal de los 10 cánceres más frecuentes en Colombia y el quinto en incidencia.1 A nivel global, se ha descrito heterogeneidad en los fenotipos de los pacientes y de su enfermedad, así como en las características genómicas de los tumores. Esto subraya la necesidad de contar con datos locales. Los pacientes con cáncer de pulmón han sido poco caracterizados en Colombia. Este estudio pretende caracterizar desde el punto de vista clínico, patológico y molecular a los pacientes con cáncer primario pulmonar atendidos en el centro de experticia en oncología torácica de una institución respiratoria en Bogotá, así como el tiempo que tardaron en ser diagnosticados y en recibir tratamiento. Reconocemos que la población atendida en un único centro no es representativa de la población general del país. Aun así, en ausencia de registros nacionales confiables, aporta información preliminar que permite aproximarse a la realidad de la patología en subregiones y centros de similares características.
Materiales y métodos:
Diseño del estudio y participantes: Fundación Neumológica Colombiana es una clínica ambulatoria en Bogotá especializada en medicina respiratoria. Tiene un servicio de neumología intervencionista que realiza broncoscopia flexible, EBUS radial y lineal, y broncoscopia rígida. En 2019, se constituyó la junta multidisciplinar de tumores de tórax y el servicio de neumología oncológica, una consulta especializada en tamizaje, seguimiento de nódulos pulmonares, abordaje diagnóstico y estadificación de cáncer pulmonar, y manejo complementario de comorbilidades pulmonares de pacientes con cáncer. La mayoría de los pacientes residen en Bogotá o municipios aledaños y realizan aportes económicos al sistema de salud. Por particularidades del sistema público de salud de Colombia, los pacientes son remitidos a nuestro servicio en momentos distintos de su enfermedad y no siempre se tiene continuidad en el seguimiento. Además, realizan sus estudios de imágenes diagnósticas, inmunohistoquímica, biología molecular, procedimientos quirúrgicos y tratamientos oncológicos en diferentes instituciones externas.
Se incluyeron todos los pacientes mayores de 18 años con cáncer primario pulmonar de cualquier histología, con excepción del linaje hematolinfoide, que asistieron a al menos una consulta con el servicio de neumología oncológica entre enero de 2019 y agosto de 2023. Se requería confirmación diagnóstica con histopatología básica; sin embargo, si el cuadro clínico, histológico e imagenológico era consistente con un origen primario pulmonar a criterio de su médico tratante, no era indispensable la inmunohistoquímica. Se excluyeron pacientes con confirmación o sospecha de origen extrapulmonar. Se incluyeron casos con diagnósticos externos y previamente tratados.
Los candidatos se identificaron en la base de datos de pacientes atendidos en el servicio. Se realizó revisión retrospectiva de sus historias clínicas entre agosto y noviembre de 2023.
Variables
Todas las variables hacen referencia a la condición del paciente al momento del diagnóstico. Historia de consumo de tabaco se definió como haber consumido al menos 100 cigarrillos en la vida. Exposición a humo de biomasa (leña o carbón) se definió como haber estado expuesto a este humo de forma regular, la mayoría de los días de la semana, por al menos 10 años. Antecedente personal de cáncer excluyó cánceres de piel distintos a melanoma.
Se determinó el estadio tumoral con la mejor información disponible, que debía incluir como mínimo un TAC de tórax contrastado con extensión a abdomen superior, e idealmente también PET-CT 18-FDG, EBUS lineal en lesiones > 3cm, centrales, o clasificadas como N≥1 por TAC y/o PET, y RMN cerebral si la estadificación por las modalidades previas era ≥ IB. De estar disponible, se prefirió el estadio patológico sobre el clínico.
En concordancia con lo establecido por la Cuenta de Alto Costo para Colombia en 2018,2 se definió la “fecha de sospecha” como el día de la primera consulta médica en que se sospechó cáncer pulmonar con remisión al especialista y la “fecha de diagnóstico” como la fecha en que se firmó el reporte de la patología que confirmó el diagnóstico. Sin embargo, anticipando una alta proporción de datos faltantes, se plantearon a priori subrogados que correspondían a fechas conceptualmente relacionadas, relativamente cercanas y bien definidas, con mayor probabilidad de haber sido registradas en la historia clínica. Así, de no conocerse las anteriores fechas, se podía tomar como “fecha de sospecha” el día de realización de la imagen radiológica considerada sospechosa y la “fecha de diagnóstico” como el día en que se realizó el procedimiento de la biopsia. El tiempo al diagnóstico se definió como los días transcurridos entre la sospecha y el diagnóstico; y el tiempo al tratamiento, entre el diagnóstico y el primer tratamiento para cáncer que incluyó: resección oncológica, pleurodesis paliativa, radioterapia en lesión principal, radioterapia cerebral, metastasectomía con intención terapéutica y terapias oncológicas sistémicas.
Los tumores primarios del pulmón se clasificaron en 3 categorías: 1) tumores epiteliales malignos, comúnmente conocidos como carcinomas pulmonares de célula no pequeña (CPCNP), 2) tumores neuroendocrinos (TNE), también conocidos como carcinoides, y 3) carcinomas neuroendocrinos (CNE) que incluyen el carcinoma de célula pequeña y el carcinoma neuroendocrino de célula grande.3 En el subgrupo con CPCNP, si estaban disponibles, se registraron los estudios para mutaciones en los genes EGFR, ALK, ROS 1, BRAF, RET, MET, NTRK, HER-2 y KRAS, y la expresión de PD-L1. Las mutaciones de los primeros 7 genes se consideraron accionables por contar con terapias dirigidas aprobadas y recomendadas por guías de práctica clínica internacionales para su uso en primera línea.4 La expresión de PD-L1 se registró como la proporción de marcador tumoral (TPS, por sus siglas en inglés) y se consideró alta expresión un TPS > 50%. Cuando los estudios fueron solicitados desde la consulta de neumología oncológica institucional, fueron remitidos al laboratorio de biología molecular FICMAC, que inicialmente ofertó en tejido PCR para EGFR e inmunohistoquímica para ALK y PD-L1 (clona SP263), y posteriormente incluyó otros genes en tejido y EGFR por PCR en sangre periférica. La definición operativa de otras variables clínicas puede consultarse en el material suplementario.
Análisis estadístico
Se usó el software estadístico STATA 16. Se realizó un análisis por medio de gráficos para evaluar asimetría, dispersión y datos externos o atípicos. Las variables cualitativas se describieron como frecuencias y porcentajes, y las variables cuantitativas con medidas de tendencia central y de dispersión de acuerdo con el supuesto de normalidad evaluado por la prueba de Shapiro-Wilk.
Se exploró la relación entre: 1) Historia de consumo de tabaco y sexo. 2) En CPCNP con perfilamiento molecular, la presencia de mutaciones accionables o alta expresión de PD-L1, por un lado; y sexo, edad, exposición a tabaco o biomasa, antecedentes oncológicos e histología, por otro lado. Se usaron las pruebas de Chi cuadrado (χ²) o test exacto de Fisher para las variables cualitativas y las pruebas t de Student o U de Mann-Whitney para las variables cuantitativas, de acuerdo con su distribución. Todas las pruebas se evaluaron a un nivel de significancia de 0,05 a 2 colas.
Aspectos éticos
Se obtuvo aprobación del Comité de Ética en Investigación de la Fundación Neumológica Colombiana y se cumplieron las buenas prácticas clínicas y los principios establecidos en la Declaración de Helsinki. Se garantizó la confidencialidad de los datos de los participantes de acuerdo con la ley de protección de datos personales en Colombia y las regulaciones nacionales sobre investigación en salud establecidas en la Resolución 8430 de 1993 del Ministerio de Salud. Se aseguró la privacidad y anonimización de la información de los pacientes.
Resultados
Se identificaron 167 pacientes candidatos. Se excluyeron 4 pacientes: uno sin confirmación histológica, uno cuya información clínica básica estaba muy incompleta, uno con diagnóstico final de metástasis pulmonar de cáncer de cérvix y uno que tenía menos de 18 años al momento del diagnóstico. Los 163 pacientes restantes fueron analizados.
Las características demográficas y clínicas de los pacientes se describen en la Tabla 1. Hubo predominio del sexo femenino con 59,5%. El 50,3% de los sujetos tenían antecedente de consumo de tabaco. Entre las mujeres hubo menor prevalencia de historia de consumo de tabaco en comparación con los hombres (35,1% vs 72,7%, p<0,001). (Tabla S1) No hubo diferencias estadísticamente significativas en la intensidad de consumo de tabaco medida por índice paquete- año (IPA) entre las mujeres y los hombres que habían fumado. (Tabla S2 y Figura S1). El 38,7% de los pacientes no tenía ninguna exposición de riesgo (tabaco, humo de leña, sílice o asbesto).
Tabla 1.
Características demográficas y clínicas de los pacientes con cáncer primario de pulmón.
|
N = 163 |
|
|
Edad, años |
67,0 ± 11,8 |
|
Sexo, femenino |
97 (59,5) |
|
IMC, kg/m2 |
24,7 ± 4,2 |
|
Antecedentes exposicionales |
|
|
Ningún antecedente |
63 (38,7) |
|
Historia de consumo de tabaco |
82 (50,3) |
|
IPA entre quienes habían fumadoa |
20,0 (10,0 – 32,5) |
|
Exposición a humo de biomasa |
28 (17,2) |
|
Exposición a sílice |
4 (2,5) |
|
Exposición a asbesto |
1 (0,6) |
|
Antecedentes oncológicos |
|
|
Antecedente personal de cáncer |
37 (22,7) |
|
Tipo de cáncer |
37 (100) |
|
Mama |
9 (24,3) |
|
Piel no melanoma |
7 (18,9) |
|
Próstata |
6 (16,2) |
|
Tiroides |
6 (16,2) |
|
Cérvix |
5 (13,5) |
|
Colon y recto |
2 (5,4) |
|
Vejiga |
2 (5,4) |
|
Pulmón |
1 (2,7) |
|
Linfoma no Hodgkin |
1 (2,7) |
|
Melanoma |
1 (2,7) |
|
GIST |
1 (2,7) |
|
Familiar en 1° grado con cáncer pulmonar |
4 (2,5) |
|
Comorbilidades cardiopulmonares |
|
|
Ninguna |
95 (58,3) |
|
Falla cardíaca |
3 (1,8) |
|
Enfermedad coronaria |
19 (11,7) |
|
EPOC |
40 (24,5) |
|
Enfisema |
32 (19,6) |
|
EPID |
9 (5,5) |
|
Alta probabilidad de hipertensión pulmonar |
20 (12,3) |
Valores como n (%), media ± DE o mediana (p25 – p75); IMC: índice de masa corporal. IPA: índice paquete-año. EPOC: enfermedad pulmonar obstructiva crónica. EPID: enfermedad pulmonar intersticial difusa. GIST: tumor estromal gastrointestinal. a: en su cálculo se excluyeron 7 pacientes con datos faltantes.
El 18,5% de los pacientes tenía antecedente previo de cáncer; el 33,1% tenía al menos una comorbilidad pulmonar y el 20,2% tenía al menos una comorbilidad cardíaca. La condición funcional respiratoria de los pacientes a quienes se les realizaron pruebas se describe en la Tabla 2. El dato que se pudo obtener de la mayor cantidad de pacientes (94%) fue que el 27,5% usaba o se le había prescrito oxigenoterapia domiciliaria. El 36,4% de las espirometrías y el 39,8% de las DLCO realizadas mostraron algún grado de deterioro funcional.
Tabla 2.
Función pulmonar de los pacientes con cáncer primario de pulmón.
|
Uso de oxígeno domiciliario |
N =153 |
|
Sí |
42 (27,5) |
|
Espirometría |
N =107 |
|
Anormal |
39 (36,4) |
|
Tipo de anormalidad, obstructiva |
28 (71,8) |
|
VEF1 (% del predicho) |
90,7 ± 21,8 |
|
VEF1 < 70 % |
15 (14,3) |
|
DLCO ajustada a la altura (DLCOaj) |
N = 88 |
|
Disminuida |
35 (39,8) |
|
DLCOaj (% del predicho) |
77,9 ± 23,7 |
|
DLCOaj < 60% |
19 (21,8) |
|
Gases arteriales al ambiente |
N = 48 |
|
PaO2 (mmHg) |
57,3 ± 6,5 |
|
PaO2 < 60 mmHg |
30 (62,5) |
|
PaCO2 (mmHg) |
33,1 ± 3,7 |
|
PaCO2 ≥ 39 mmHg |
3 (6,3) |
|
Caminata de 6 minutos |
N = 48 |
|
Distancia (m) |
491 ± 96 |
|
Desaturación basal |
9 (18,8) |
|
Desaturación solo con el ejercicio |
12 (25,0) |
Valores como n (%) o media ± DE. Los porcentajes de las variables categóricas son respecto a los pacientes a quienes se les hizo el examen.
La clasificación histológica y los estadios tumorales se detallan en la Tabla 3. El tipo de cáncer más frecuente fue el CPCNP (144 /163; 88,3%), seguido de los TNE (11/163; 6,7%) y los CNE (7/163; 4,3%). La Tabla 4 resume las características de cada tipo de cáncer pulmonar. Hubo 2 mujeres con tumor carcinoide típico multifocal, una de ellas con hiperplasia difusa idiopática de células neuroendocrinas.
Tabla 3.
Características oncológicas de los pacientes con cáncer primario pulmonar.
|
N=163 |
|
|---|---|
|
Subtipo histológico |
|
|
Carcinoma pulmonar de célula no pequeña |
144 (88,3) |
|
Adenocarcinoma |
110 (67,5) |
|
Carcinoma escamocelular |
29 (17,8) |
|
Célula no pequeña NOS |
4 (2,5) |
|
Carcinoma adenoescamoso |
1 (0,6) |
|
Tumores neuroendocrinos |
11 (6,7) |
|
Tumor carcinoide típico |
7 (4,3) |
|
Tumor carcinoide típico multifocal |
2 (1,2) |
|
Tumor carcinoide atípico |
2 (1,2) |
|
Carcinomas neuroendocrinos |
7 (4,3) |
|
Carcinoma de célula pequeña |
6 (3,7) |
|
Carcinoma neuroendocrino de célula grande |
1 (0,6) |
|
No establecido |
1 (0,6) |
|
Estadio al diagnóstico |
|
|
Temprano |
53 (32,5) |
|
0 |
2 (1,2) |
|
IA1 |
9 (5,5) |
|
IA2 |
7 (4,3) |
|
IA3 |
7 (4,3) |
|
IB |
10 (6,1) |
|
IIA |
8 (4,9) |
|
IIB |
10 (6,1) |
|
Localmente avanzado |
38 (23,3) |
|
IIIA |
14 (8,6) |
|
IIIB |
15 (9,2) |
|
IIIC |
9 (5,5) |
|
Metastásico |
68 (41,7) |
|
IVA |
36 (22,1) |
|
IVB |
32 (19,6) |
|
No establecido |
4 (2,5) a |
Valores como n (%); a. Incluye 2 pacientes con tumor carcinoide multifocal en quienes se consideró que el estadiaje convencional no era un descriptor apropiado. La estadificación es de acuerdo con la 8° edición del TNM.
Tabla 4.
Características de los pacientes con cáncer pulmonar según el tipo de tumor.
|
CNE |
CPCNP |
TNE |
|
|---|---|---|---|
|
N=7 |
N=144 |
N=11 |
|
|
Demografía |
|||
|
Edad (años) |
69,4 ± 12,8 |
67,6 ± 11,1 |
60,7 ± 16,5 |
|
Sexo masculino |
5 (71,4) |
59 (41,0) |
2 (18,2) |
|
Factores de riesgo |
|||
|
Ninguno de exposición |
1 (14,3) |
54 (37,5) |
7 (63,6) |
|
Historia de consumo de tabaco |
5 (71,4) |
73 (50,7) |
4 (36,4) |
|
IPA entre quienes habían fumado |
20 (17,5 - 35,0) |
21,5 (10,0 - 38,8) |
10 (2,0 - 10,0) |
|
Exposición a humo de biomasa |
2 (28,6) |
25 (17,4) |
1 (9,1) |
|
Antecedentes oncológicos |
|||
|
Antecedente personal de cáncer |
1 (14,3) |
34 (23,6) |
2 (18,2) |
|
Familiar en 1° grado con cáncer pulmonar |
0 (0,0) |
1 (0,7) |
3 (27,3) |
|
Comorbilidad |
|||
|
Comorbilidad cardiopulmonar a |
4 (57,1) |
62 (43,1) |
1 (9,1) |
|
Estadio |
|||
|
0 - I |
- |
30 (20,8) |
5 (45,4) |
|
II |
- |
15 (10,4) |
3 (27,3) |
|
III |
2 (28,6) |
36 (25,0) |
0 (0,0) |
|
IV |
5 (71,4) |
62 (43,1) |
1 (9,1) |
|
Desconocido |
- |
1 (0,7) |
b 2 (18,2) |
|
Función pulmonar |
|||
|
Uso de oxígeno domiciliario |
N=7 |
N=134 |
N=11 |
|
Sí |
5 (71,4) |
36 (26,9) |
1 (9,1) |
|
Espirometría |
N=4 |
N=95 |
N=7 |
|
Anormal |
2 (50) |
32 (33,7) |
4 (57,1) |
|
Tipo de anormalidad – Razón |
|||
|
obstructiva : no obstructiva |
2:00 |
3,6:1 |
1:03 |
|
DLCO |
N=3 |
N=78 |
N=6 |
|
Disminuida |
2 (66,6) |
31 (39,7) |
1 (16,7) |
Valores como n (%), media ± DE o mediana (p25-p75); CPCNP: Carcinoma Pulmonar de Célula No Pequeña. CNE: carcinomas neuroendocrinos. TNE: tumores neuroendocrinos. a. Comorbilidad cardiopulmonar: diagnóstico de enfermedad Pulmonar Obstructiva Crónica (EPOC), enfisema, Enfermedad Pulmonar Intersticial Difusa (EPID), enfermedad coronaria significativa, falla cardíaca o alta probabilidad ecocardiográfica de hipertensión pulmonar. b. 2 pacientes con tumor carcinoide multifocal en quienes se consideró que la estadificación TNM convencional no era un descriptor apropiado.
En la Tabla 5 se describe el perfilamiento molecular de los CPCNP. 81 pacientes fueron estudiados para mutaciones de EGFR, 58 de ellos para EGFR y ALK, y 37 de estos últimos para EGFR, ALK y otros genes. Se identificó al menos una mutación accionable en el 51,9% (42/81) de estos pacientes. Hubo un caso con dos mutaciones accionables: EGFR Ex19del y ALK. La presencia de mutaciones accionables se asoció con histología de adenocarcinoma (OR 6,9; p= 0,011) y sexo femenino (OR 5,8; p=0,001). (Tabla S3) Hubo una tendencia a menor prevalencia de consumo de tabaco en el grupo de pacientes con mutaciones accionables, aunque esta diferencia no fue estadísticamente significativa (OR 2,33; p=0,06). (Tabla S3) Al comparar altos y bajos expresores de PD-L1, no se observaron diferencias estadísticamente significativas en variables clínicas o patológicas. (Tabla S4)
Tabla 5.
Perfilamiento molecular de los CPCNP.
|
Marcador o gen |
Resultado |
N=144 |
|---|---|---|
|
EGFR a |
Evaluados |
81 (56,3) |
|
Mutados |
34 (42,0) |
|
|
Tipo de mutación |
||
|
Ex19del |
18 (52,9) |
|
|
Ex21L858R |
7 (20,6) |
|
|
Ex20ins |
5 (14,7) |
|
|
Ex18delE709_T710insD |
1 (2,9) |
|
|
Ex19ins |
1 (2,9) |
|
|
Mut. puntual codón 861 |
1 (2,9) |
|
|
Desconocida |
1 (2,9) |
|
|
ALK b |
Evaluados |
58 (40,3) |
|
Mutados |
4 (6,9) |
|
|
ROS1 b |
Evaluados |
37 (25,7) |
|
Mutados |
1 (2,7) |
|
|
KRAS b |
Evaluados |
27 (18,8) |
|
Mutados |
4 (14,8) |
|
|
BRAF V600 b |
Evaluados |
23 (16,0) |
|
Mutados |
2 (8,7) |
|
|
RET b |
Evaluados |
26 (18,1) |
|
Mutados |
1 (3,9) |
|
|
MET b |
Evaluados |
26 (18,1) |
|
Mutados |
1 (3,9) |
|
|
HER-2 b |
Evaluados |
26 (18,1) |
|
Mutados |
0 (0) |
|
|
NTRK b |
Evaluados |
28 (19,4) |
|
Mutados |
0 (0) |
|
|
PD-L1 |
Evaluados |
58 (40,3) |
|
Nivel de expresión |
||
|
TPS <1% |
39 (67,2) |
|
|
TPS 1-49% |
7 (12,1) |
|
|
TPS ≥ 50% |
12 (20,7) |
Valores como n (%); TPS: Tumor Proportion Score. a. Para EGFR, 60 (74,1%) pacientes tenían evaluación en tejido tumoral, 14 (17,3%) sólo tenían evaluación en sangre periférica y en 7 (8,6%) no hubo claridad del tipo de muestra evaluada. b. En la evaluación de genes diferentes a EGFR, 5 pacientes tenían NGS en sangre periférica y el resto corresponden a estudios en tejido tumoral.
El tiempo al diagnóstico se pudo calcular en 85,3% de los casos y fue ≤ 30 días en 25,9% de ellos. El tiempo al tratamiento se pudo calcular en 63,8% de los casos y fue ≤ 30 días en 40,4% de ellos. Excluyendo los pacientes para quienes un mismo procedimiento quirúrgico fue diagnóstico y terapéutico (en quienes el tiempo al tratamiento fue de 0 días), el tiempo al tratamiento fue ≤ 30 días en 15,1%. El tiempo entre la sospecha clínica y el tratamiento fue ≤ 60 días en 17,7% de los casos en que se pudo calcular. (Figura 1)
Figura 1.
Oportunidad al diagnóstico y al tratamiento de los pacientes con cáncer primario de pulmón.
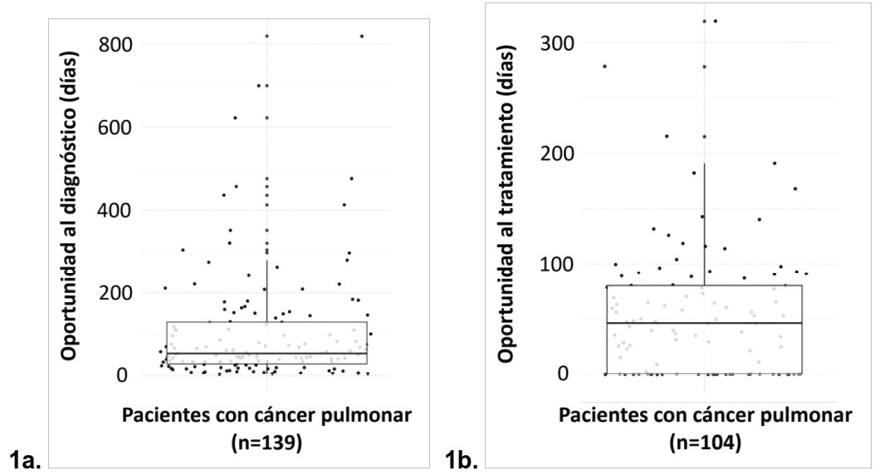
1a. Los puntos representan los días transcurridos entre la sospecha de cáncer pulmonar y su confirmación diagnóstica mediante histopatología. La línea gruesa representa la mediana (54 días) y la caja el rango intercuartílico (28 a 130 días). 1b. Los puntos representan los días transcurridos entre la confirmación diagnóstica y el inicio del primer tratamiento oncológico. La línea gruesa representa la mediana (46 días) y la caja el rango intercuartílico (0 a 80 días).
Discusión
La proporción de mujeres entre los pacientes con cáncer pulmonar encontrada en este estudio (59,5%) es mayor a lo reportado en los estudios previos en el país de entre 35,4% y 55,4%;5-10 y al 49,6% reportado por la Cuenta de Alto Costo para 2021.11 Aunque previamente se consideraba una patología predominantemente de hombres, en Estados Unidos y otras partes del mundo se ha descrito un aumento en la proporción de mujeres en los últimos 20 años.12 Igualmente, es llamativa la alta proporción de pacientes sin historia de consumo de tabaco (49,7%), mayor a lo reportado en la mayoría de los estudios previos en el país, que oscila entre 9,2% y 52,5%.5-10 Es superior al 12,5% reportado en Estados Unidos para el periodo 2011 – 2016 y al 45% reportado en China para el periodo 2014 – 2017.13-15
Preocupa que al menos 73% de los pacientes de este estudio no habrían sido elegibles para un programa de tamizaje porque nunca fumaron o tenían un IPA < 20.16 Es necesario identificar factores de riesgo diferentes al consumo de tabaco y posteriormente evaluar su rendimiento como criterio de inclusión en programas de tamizaje. En este estudio, tras indagar por exposición a sílice, asbesto o humo de biomasa, persistió un 38,7% de pacientes en quienes no se encontró ninguna exposición de riesgo. Los resultados finales del estudio TALENT en curso en Taiwan, que tamiza población con factores de riesgo distintos al IPA > 20, podrían ser de interés para nuestro país; sin embargo, el principal factor de riesgo evaluado en el TALENT es la historia familiar de cáncer pulmonar y en nuestro estudio este factor de riesgo fue raro (2,5%).17 El compromiso de la función pulmonar fue frecuente, aunque los datos faltantes no permiten estimar con confianza la proporción.
Las neoplasias neuroendocrinas representaron el 11% del total de cánceres primarios pulmonares. Se ha descrito previamente que los pacientes con CNE en su mayoría son hombres, tienen historia de consumo de tabaco, se diagnostican en estadios avanzados y tienen alta prevalencia de comorbilidad cardiopulmonar.18 Por otro lado, se ha descrito que los pacientes con TNE mayoritariamente son mujeres, no tienen historia de consumo de tabaco y se diagnostican en estadios tempranos.19,20 Los hallazgos de este estudio son consistentes con dichas características, aunque la pequeña cantidad de pacientes no permite hacer comparaciones formales.
Entre los pacientes con CPCNP, el estadio más frecuente al diagnóstico fue el IV con 43,1%, cifra inferior al 78,8% que reportó el Instituto Nacional de Cancerología entre 2013 y 2018;10 y al 74,1% reportado por la Cuenta de Alto Costo para Colombia en 2021.11 Por otro lado, 20,8% fueron estadio I. Tanto nuestras cifras como las de otros centros resaltan la importancia de continuar implementando estrategias que promuevan el diagnóstico en estadios tempranos.
La baja proporción de pacientes con CPCNP que contaban con perfilamiento molecular básico (56,3%) se debió a una combinación de barreras en el acceso, agotamiento del tejido de biopsias y a que, antes de septiembre 2020, cuando se publicó el estudio ADAURA, no había una indicación fuerte de realizar perfilamiento molecular en tumores resecables, pues no cambiaba la conducta terapéutica. La alta prevalencia de mutaciones de EGFR (42%) y mutaciones accionables (51,9%) encontrada puede deberse en parte a sesgo de selección ya que el subgrupo de pacientes testeados tenía proporciones de mujeres, histología de adenocarcinoma y personas sin historia de consumo de tabaco (65,5%, 85,1% y 56,8%, respectivamente) mayores al del grupo total de pacientes con CPCNP (59,0%, 76,4% y 49,3%, respectivamente); y estas 3 son variables que se asocian a la presencia de mutaciones accionables.21 El estudio más grande en el país evaluó 1.939 pacientes y encontró una menor prevalencia de mutaciones de EGFR de 24,7%, a pesar de que incluyó una proporción similar de mujeres (63,3%), mayores proporciones de personas que nunca habían fumado (75,2%) y con histología de adenocarcinoma (93,2%).21
Por consenso Delphi, se ha propuesto como indicador de calidad que el tiempo hasta el diagnóstico de cáncer pulmonar sea menor a 30 días.22 Las guías canadienses recomiendan que, en el caso de los tumores resecables, el tiempo entre la primera consulta con especialista y la cirugía sea menor a 8 semanas.23 En Colombia, en 2021, la Cuenta de Alto Costo reportó para todo el país un tiempo hasta el diagnóstico de 27 días (13 - 47) y un tiempo hasta el tratamiento de 39 (19 - 68) días.11 En nuestro estudio, ambos tiempos fueron mayores. Debido a que las definiciones para fecha de sospecha y fecha de diagnóstico que plantea la Cuenta de Alto Costo no son de registro clínico rutinario, se debió recurrir en muchos casos a las fechas subrogadas propuestas desde el protocolo. Vale la pena resaltar que la Cuenta de Alto Costo se alimenta de reportes obligatorios de clínicos que probablemente enfrenten las mismas dificultades a la hora de establecer las fechas requeridas a partir de sus registros, y es posible que dichas estimaciones sean también imprecisas. Además, que dos años del estudio coincidieron con la pandemia COVID-19 y el deterioro en las condiciones del sistema de salud pudo influir negativamente en la oportunidad de la atención.
Limitaciones y fortalezas
Se deben señalar varias limitaciones del presente estudio. Como cualquier estudio monocéntrico, puede estar sujeto a sesgos de selección debido a la naturaleza de la institución y la población que atiende. Los resultados podrían ser extrapolables a otras instituciones de la región que se especialicen en medicina respiratoria y neumología intervencionista, mas no a otros contextos. Los datos faltantes en varias categorías de variables limitan la precisión de las estimaciones realizadas; aun así, se consideró valioso reportarlas ya que hay poca información previa en Colombia. Nuevos estudios con recolección prospectiva de los datos podrían lograr una caracterización más exacta.
El tamaño reducido de la muestra limitó el poder del estudio para detectar asociaciones significativas o realizar análisis de subgrupos. Aun así, los resultados obtenidos son consistentes con lo reportado en la literatura internacional. Entre las fortalezas del estudio, se destaca el uso de datos clínicos detallados obtenidos de manera sistemática, lo cual minimiza la posibilidad de sesgos de información y favorece a la confiabilidad de los hallazgos presentados.
Conclusiones
En nuestro centro, se documentó una mayor proporción de pacientes con cáncer primario pulmonar sin historia de consumo de tabaco comparado con el histórico reportado en Colombia. La proporción de pacientes con CPCNP con mutaciones accionables también fue mayor. A pesar de que los tiempos de abordaje superaron lo recomendado internacionalmente, la proporción de estadios tempranos fue mayor a lo reportado previamente en el país. Consideramos que se requiere aún fortalecer estrategias para un diagnóstico estructurado y oportuno del cáncer de pulmón que incluya acceso rutinario a perfilamiento molecular en Colombia.
Agradecimientos: a la Universidad de la Sabana por su apoyo en el desarrollo del estudio MEDEESP-5-2025.
Financiamiento: los autores declaran que el trabajo no tuvo financiamiento.
Conflictos de interés: LCSC: AstraZeneca le patrocinó en 2022 traslados aéreos y hospedaje en hotel para asistir al congreso de neumología de ALAT en Lima, Perú. HAV: participó como asesor y speaker de AstraZeneca, BMS, MSD, Merck Serono. LCVM: recibió financiación como speaker, consultora y asesora de AstraZeneca, Merck Sharp & Dome, 2024 - 2025. Los otros autores declaran que no tienen conflictos de intereses relacionados con el tema de esta publicación.
Declaración de cumplimiento ético: se obtuvo aprobación del Comité de Ética en Investigación de la Fundación Neumológica Colombiana y se cumplieron las buenas prácticas clínicas y los principios establecidos en la Declaración de Helsinki.
Contribuciones de los autores: HV participó en el análisis de los datos, la discusión y la revisión del documento final. Todos los demás autores participaron en todas las fases del estudio. Todos los autores aprobaron el documento final.
El Editor en Jefe, Dr. Francisco Arancibia, realizó el seguimiento del proceso de revisión y aprobó este artículo.
Referencias:
1. Globocan: International Agency for Research on Cancer. Colombia fact sheet 2020 [Internet]. [Consultado 18 feb 2025]. Disponible en: https://gco.iarc.who.int/media/globocan/factsheets/populations/170-colombia-fact-sheet.pdf 2. Fondo Colombiano de Enfermedades de Alto Costo Cuenta de Alto Costo [CAC]. Indicadores de gestión del riesgo en pacientes con cáncer de pulmón en Colombia, Bogotá D.C.; 2018. [Internet]. [Consultado 9 ago 2025]. Disponible en: https://cuentadealtocosto.org/consenso-basado-en-la-evidencia-indicadores-de-gestion-del-riesgo-en-pacientes-con-cancer-de-pulmon-en-colombia/ 3. Nicholson AG, Tsao MS, Beasley MB, Borczuk AC, Brambilla E, Cooper WA et al. The 2021 WHO Classification of Lung Tumors: Impact of Advances Since 2015. J Thorac Oncol 2022;17(3):362–87. https://doi.org/10.1016/j.jtho.2021.11.003 4. Bazhenova L, Ismaila N, Abu Rous F, Alluri K, Freeman-Daily J, Halmos B et al. Therapy for Stage IV Non–Small Cell Lung Cancer With Driver Alterations: ASCO Living Guideline, Version 2024.2. J Clin Oncol 2024;42(36):e72–86. https://doi.org/10.1200/jco-24-02133 5. Martínez C, Morón F, Meléndez P. Síntomas respiratorios en pacientes con cáncer pulmonar: una comparación del tiempo de consulta entre fumadores y no fumadores. Rev Colomb Neumol 2003;15(3):105–9. https://doi.org/10.30789/rcneumologia.v15.n3.2003.1245 6. Alvarado-Sarzosa F, Martinez-Jaramillo SI, García-Herreros-Hellal LG, Beltrán-Jimenez RJ, Zuluaga-Restrepo JD, Parra-Medina R et al. Desenlaces clínicos de pacientes con cáncer de pulmón de célula no pequeña temprano manejados quirúrgicamente en Bogotá. Rev Colomb Cancerol 2023;27(2):240–50. https://doi.org/10.35509/01239015.904 7. Otero JM, Cardona AF, Revéiz L, Campo F, Carranza H, Vargas CA et al. Supervivencia en pacientes con adenocarcinoma de pulmón metastásico y registro de las primeras mutaciones en el receptor para el factor de crecimiento epidérmico documentado en Colombia Estudio del ONCOLGroup. Acta Médica Colombiana 2009;34(2):55–65. 8. Lema M, Preciado B, Lema C, Rodríguez D, Pineda M, Egurrola J et al. Survival Outcomes in Advanced Non-Small Cell Lung Cancer in a Cancer Center in Medellin - Colombia. CES Medicina 2023;37(1):44–57. https://doi.org/10.21615/cesmedicina.7186 9. Martin C, Cuello M, Barajas O, Recondo G, Aruachan S, Perroud H et al. Real-world evaluation of molecular testing and treatment patterns for EGFR mutations in non-small cell lung cancer in Latin America. Mol Clin Oncol 2022;16(6):1–10. https://doi.org/10.3892/mco.2021.2439 10. Alarcón ML, Brugés R, Carvajal C, Vallejo C, Beltrán R. Características de los pacientes con cáncer de pulmón de célula no pequeña en el Instituto Nacional de Cancerología de Bogotá. Rev Col Cancerol 2021;25(2):103–9. https://doi.org/10.35509/01239015.706 11. Fondo Colombiano de Enfermedades de Alto Costo Cuenta de Alto Costo (CAC). Situación del cáncer en la población adulta atendida en el SGSSS de Colombia 2022. Bogotá, D.C.; 2023. 12. Fu Y, Liu J, Chen Y, Liu Z, Xia H, Xu H. Gender disparities in lung cancer incidence in the United States during 2001–2019. Sci Rep 2023;13(12581):1–14. https://doi.org/10.1038/s41598-023-39440-8 13. Huang C, Qu X, Du J. Proportion of lung adenocarcinoma in female never-smokers has increased dramatically over the past 28 years. J Thorac Dis 2019;11:2685–8. https://doi.org/10.21037/jtd.2019.07.08 14. Siegel DA, Fedewa SA, Henley SJ, Pollack LA, Jemal A. Proportion of Never Smokers Among Men and Women With Lung Cancer in 7 US States. JAMA Oncol 2021;7(2):302–4. https://doi.org/10.1001/jamaoncol.2020.6362 15. Shiels MS, Graubard BI, McNeel TS, Kahle L, Freedman ND. Trends in smoking-attributable and smoking-unrelated lung cancer death rates in the United States, 1991-2018. JNCI 2023;0(0):1–6. https://doi.org/10.1093/jnci/djad256 16. Adams SJ, Stone E, Baldwin DR, Vliegenthart R, Lee P, Fintelmann FJ. Lung cancer screening. The Lancet 2023;401(10374):390–408. https://doi.org/10.1016/S0140-6736(22)01694-4 17. Chang GC, Chiu CH, Yu CJ, Chang YC, Chang YH, Hsu KH et al. Low-dose CT screening among never-smokers with or without a family history of lung cancer in Taiwan: a prospective cohort study. Lancet Respir Med 2024;12(2):141–52. https://doi.org/10.1016/S2213-2600(23)00338-7 18. Franco F, Carcereny E, Guirado M, Ortega AL, López-Castro R, Rodríguez-Abreu D et al. Epidemiology, treatment, and survival in small cell lung cancer in Spain: Data from the thoracic tumor registry. PLoS One 2021;16(6):e0251761. https://doi.org/10.1371/journal.pone.0251761 19. Taboada Barrios LB, López Panqueva R del P, García-Herreros Hellal LG, Gonzalez Devia D. Experiencia diagnóstica de diez años del tumor neuroendocrino de pulmón en la Fundación Santafé de Bogotá 2001-2010. Rev Col Neumol 2001;24(2):84–91. https://doi.org/10.30789/rcneumologia.v24.n2.2012.189 20. Papaxoinis G, Lamarca A, Quinn AM, Mansoor W, Nonaka D. Clinical and Pathologic Characteristics of Pulmonary Carcinoid Tumors in Central and Peripheral Locations. Endocr Pathol 2018;29:259–68. https://doi.org/10.1007/s12022-018-9530-y 21. Arrieta O, Cardona AF, Martín C, Más-López L, Corrales-Rodríguez L, Bramuglia G et al. Updated frequency of EGFR and KRAS mutations in NonSmall-cell lung cancer in Latin America: The Latin-American consortium for the investigation of lung cancer (CLICaP). J Thorac Oncol 2015;10(5):838–43. https://doi.org/10.1097/JTO.0000000000000481 22. Lynch C, Harrison S, Butler J, Baldwin DR, Dawkins P, van der Horst J et al. An International Consensus on Actions to Improve Lung Cancer Survival: A Modified Delphi Method Among Clinical Experts in the International Cancer Benchmarking Partnership. Cancer Control 2022;29. https://doi.org/10.1177/10732748221119354 23. Labbé C, Anderson M, Simard Msc S, Tremblay L, Laberge F, Vaillancourt R et al. Wait times for diagnosis and treatment of lung cancer: A single-centre experience. Current Oncology 2017;24(6):367–73. https://doi.org/10.3747/co.24.3655Material suplementario:
Tabla S1.
Historia de consumo de tabaco en hombres y mujeres con cáncer primario pulmonar.
|
Femenino |
Masculino |
Población total |
Valor p |
|
|
N=97 |
N=66 |
N=163 |
||
|
Nunca fumó |
63 (64,9) |
18 (27,3) |
81 (49,7) |
<0,001 |
|
Sí fumó |
34 (35,1) |
48 (72,7) |
82 (50,3) |
Valores como n (%).
Tabla S2.
IPA de hombres y mujeres con cáncer primario pulmonar e historia de consumo de tabaco.
|
Femenino |
Masculino |
Valor p |
|
|
N=31 |
N=45 |
||
|
IPA entre quienes habían fumado |
|||
|
mediana (p25-p75) |
20,0 (9,0-30,0) |
21,0 (11,5-40,0) |
0,282 |
|
media ± DE |
22,8 ± 20,7 |
30,3 ± 26,6 |
Valores como mediana (p25-p75) o media ± DE; IPA: Índice paquete-año.
Figura S1.
IPA de hombres y mujeres con cáncer primario pulmonar e historia de consumo de tabaco.
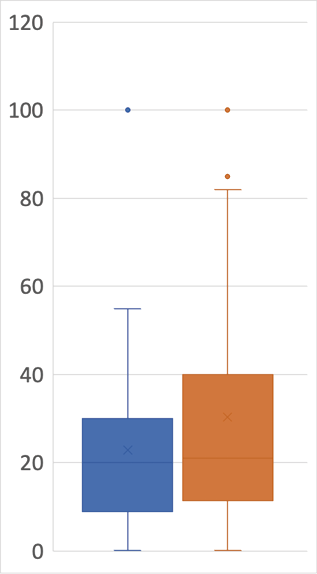
IPA: Índice paquete-año. IPA de hombres y mujeres que tenían historia de consumo de tabaco (n=76). Azul: mujeres. Naranja: hombres. La caja representa el rango intercuartílico y la línea horizontal central la mediana. Los puntos representan datos extremos.
Tabla S3.
Características clínicas y patológicas de los pacientes con CPCNP con y sin mutaciones accionables.
|
Variable |
Sin mutación accionable (Ninguna, HER-2 o KRAS) |
Con mutación accionable (EGFR, ALK, ROS1, MET, RET, BRAF, NTRK) |
Población total |
Valor p |
|
N=39 |
N=42 |
N=81 |
||
|
Variables clínicas: |
||||
|
Sexo, femenino |
18 (46,2) |
35 (83,3) |
53 (65,4) |
0,001 |
|
Edad, años |
68,5 ± 9,4 |
64,2 ± 13,8 |
66,2 ± 12,0 |
0,109 |
|
Historia de tabaquismo |
21 (53,8) |
14 (33,3) |
35 (43,2) |
0,063 |
|
IPA entre fumadores |
||||
|
mediana (p25-p75) |
20,5 (11,5 – 42,5) |
11,5 (1 – 25) |
20 (7-30) |
0,107 |
|
promedio ± DE |
27,3 ± 21,2 |
18,6 ± 26,0 |
23,7 ± 23,3 |
|
|
Exposición a biomasa |
6 (15,4) |
6 (14,3) |
12 (14,8) |
0,889 |
|
Antecedente de cáncer |
9 (23,1) |
9 (21,4) |
18 (22,2) |
0,858 |
|
Antecedente personal o |
1 (2,6) |
1 (2,4) |
2 (2,5) |
0,958 |
|
familiar de cáncer pulmonar |
||||
|
Variables patológicas: |
||||
|
Adenocarcinoma o |
||||
|
adenoescamoso (vs otros) |
29 (74,4) |
40 (95,2) |
69 (85,2) |
0,011 |
Valores como n (%), promedio ± DE o mediana (p25-p75). CPCNP: Carcinoma Pulmonar de Célula No Pequeña.
Tabla S4.
Características clínicas y patológicas de los pacientes con CPCNP con y sin alta expresión de PD-L1.
|
Variable |
PD-L1 TPS ≤ 50% |
PD-L1 TPS > 50% |
Población total |
Valor p |
|
N=46 |
N=12 |
N=58 |
||
|
Variables clínicas: |
||||
|
Sexo, femenino |
28 (60,9) |
5 (41,7) |
33 (56,9) |
0,232 |
|
Edad, años |
66,5 ± 13,3 |
67,5 ± 8,4 |
66,7 ± 12,4 |
0,977 |
|
Historia de tabaquismo |
25 (54,4) |
7 (58,3) |
32 (55,2) |
0,805 |
|
IPA entre fumadores |
||||
|
mediana (p25-p75) |
18 (9 – 29) |
37,5 (25 – 55) |
20 (10 - 30) |
0,107 |
|
promedio ± DE |
22,2 ± 20,8 |
35,8 ± 22,2 |
24,9 ± 21,49 |
|
|
Exposición a biomasa |
7 (15,2) |
2 (16,6) |
(15,5) |
0,902 |
|
Antecedente de cáncer |
13 (28,3) |
0 (0) |
13 (22,4) |
0,051 |
|
Antecedente personal o |
1 (2,2) |
0 (0) |
1 (1,7) |
0,606 |
|
familiar de cáncer pulmonar |
||||
|
Variables patológicas: |
||||
|
Adenocarcinoma o |
||||
|
adenoescamoso (vs otros) |
38 (82,6) |
7 (58,3) |
45 (77,6) |
0,073 |
Valores como n (%), promedio ± DE o mediana (p25-p75). TPS: Tumor Proportion Score. CPCNP: Carcinoma Pulmonar de Célula No Pequeña.
Definiciones operativas de las variables del estudio:
- Historia de consumo de tabaco: consumo de al menos 100 cigarrillos en la vida.
- Índice paquete año (IPA): (cantidad promedio de cigarrillos consumidos por día) × (número de años de consumo) / 20.
- Exposición a humo de combustión de biomasa (leña, carbón): exposición en recinto cerrado o abierto de forma regular la mayoría de días de la semana por al menos 10 años.
- Exposición a sílice: laborar por al menos 5 años en actividades que se han descrito como relacionadas al desarrollo de silicosis como construcción, canteras o minas.
- Exposición a asbesto: haber laborado (sin importar la duración) en actividades con uso u exposición conocida a productos de asbesto como mecánica automotriz, plomería o demolición.
- Historia familiar de cáncer de pulmón: presencia de familiares en primer grado de consanguinidad con el diagnóstico de cáncer de pulmón.
- Enfermedad coronaria: historia de revascularización percutánea o quirúrgica, o reporte de cateterismo con obstrucción de > 50% de la coronaria izquierda o > 70% de otra arteria principal.
- Falla cardíaca: antecedente referido por el paciente y registrado así en la historia o evidencia ecocardiográfica de FEVI < 40%.
- Enfermedad pulmonar obstructiva crónica (EPOC): espirometría con relación Volumen Espiratorio Forzado en el primer segundo (FEV1, por su sigla en inglés) / Capacidad Vital Forzada (FVC, por su sigla en inglés) inferior al límite inferior de la normalidad (LIN) asociado a historia de exposición a cigarrillo con IPA > 10 o a humo de leña de acuerdo a lo definido previamente.
- Enfisema: Descripción en la historia clínica del hallazgo radiológico, bien sea como transcripción de la interpretación del radiólogo o como interpretación del neumólogo tratante.
- Enfermedad pulmonar intersticial (EPID): diagnóstico registrado en la historia clínica por el neumólogo tratante posterior a evaluación de una imagen tomográfica.
- Hipertensión pulmonar: presencia de un ecocardiograma con PSAP > 40 mmHg o que reúne los siguientes criterios: velocidad máxima de regurgitación tricuspídea > 2,8 m/seg y al menos un signo indirecto de hipertensión pulmonar. En ausencia de regurgitación tricuspídea al menos 2 signos indirectos de hipertensión pulmonar, siendo uno de ellos dilatación o disfunción sistólica del ventrículo derecho.
- Oxigenoterapia domiciliaria: registro de que el paciente usa oxígeno en casa o de que este haya sido prescrito por su neumólogo tratante. No se especifica un mínimo de horas de uso al día.
- Tiempo al diagnóstico: tiempo transcurrido en días entre la fecha de sospecha y la fecha de diagnóstico.
- Fecha de sospecha: fecha de la consulta médica en que, con base en un cuadro clínico o más frecuentemente tras revisar un reporte imagenológico, se sospechó el diagnóstico de neoplasia maligna de pulmón. En caso de que no se conociese esa fecha, se usó la fecha de realización de la primera imagen diagnóstica de pulmón que se haya considerado sospechosa de neoplasia maligna de pulmón.
- Fecha de diagnóstico: fecha en que se firmó el reporte de histopatología que confirmó el diagnóstico. En caso de que no se conociese esa fecha, se usó la fecha de toma de la biopsia.
- Tiempo al tratamiento: días transcurridos entre la fecha de diagnóstico y la fecha de inicio de tratamiento.
- Fecha de inicio de tratamiento: fecha en que se inició el primer tratamiento para cáncer que podría ser: cirugía de resección pulmonar con intención terapéutica, pleurodesis paliativa, radioterapia en lesión principal, radioterapia cerebral, metastasectomía con intención terapéutica.
- Espirometría anormal: si los valores absolutos de FEV1, FVC o relación FEV1/FVC estaban por debajo del límite inferior de la normalidad predicho de acuerdo al sexo, la edad, la talla y la raza.
- Espirometría anormal obstructiva: espirometría con VEF1/CVF inferior al límite inferior de la normalidad predicho, independientemente de si el VEF1 y/o la CVF están normales o disminuidas.
- Espirometría anormal no obstructiva: espirometría con VEF1/CVF normal y VEF1 y/o CVF por debajo del límite inferior de la normalidad predicho.
- Difusión de Monóxido de Carbono Ajustada a la altura de Bogotá (DLCOaj, por su sigla en inglés) anormal: valor inferior al límite inferior de la normalidad predicho de acuerdo al sexo, la edad, la talla y la raza.
- Desaturación basal en caminata de 6 minutos: realización de la misma con oxígeno suplementario o una SpO2 inicial al ambiente < 88%.
- Desaturación con el ejercicio en caminata de 6 minutos: una SpO2 inicial ≥ 88% con SpO2 final < 85%, ambas al aire ambiente.
- Mutación accionable: las mutaciones de EGFR, ALK, ROS 1, BRAF, RET, MET y NTRK se consideraron accionables por contar con terapias dirigidas aprobadas y recomendadas por guías de práctica clínica internacionales para su uso en primera línea.
- Alta expresión de PD-L1: Puntaje de proporción tumoral (TPS, por su sigla en inglés) > 50%.